题目内容
17. 人们研究金星大气成分,发现金星大气中有一种称之为羰基硫(COS)的分子,已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是( )
人们研究金星大气成分,发现金星大气中有一种称之为羰基硫(COS)的分子,已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是( )| A. | 羰基硫属于非极性分子 | |
| B. | 羰基硫的电子式为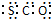 | |
| C. | 羰基硫的沸点比CO2低 | |
| D. | 羰基硫分子中三个原子处于同一直线上 |
分析 A.极性分子中正负电荷的中心不重合;
B.根据羰基硫分子中所有原子的最外层都满足8电子结构判断其电子式;
C.组成和结构相似的分子,相对分子质量越大,分子间作用力越强,熔沸点越高;
D.根据二氧化碳的结构判断羰基硫的结构.
解答 解:A.羰基硫正负电荷的中心不重合,是极性分子,故A错误;
B.羰基硫分子中所有原子的最外层都满足8电子结构,则羰基硫的电子式为: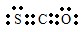 ,故B错误;
,故B错误;
C.组成和结构相似的分子,相对分子质量越大,分子间作用力越强,熔沸点越高,羰基硫(COS)的相对分子质量比二氧化碳的大,则羰基硫的沸点比CO2高,故C错误;
D.二氧化碳结构对称,是直线型分子,所以羰基硫也是直线型分子,但2个极性键的极性不等,所以正负电荷的中心不重合,是极性分子,故D正确;
故选D.
点评 本题考查物质结构与性质,根据二氧化碳的结构解答,学会迁移应用是解题的关键,注意掌握电子式的书写方法.

练习册系列答案
相关题目
8.下列反应中,符合能量变化如图所示的反应是( )
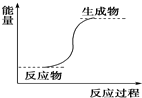

| A. | Ba(OH)2•8H2O与NH4Cl反应 | B. | 铝与稀盐酸 | ||
| C. | NaOH与HCl的反应 | D. | 甲烷与O2的燃烧反应 |
12.电浮选凝聚法是工业上采用的一种污水处理方法,某研究小组用电浮选凝聚法处理污水,设计装置如图所示,下列说法正确的是( )
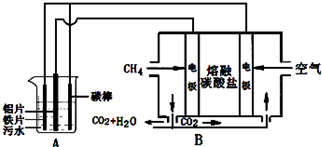

| A. | 装置A中碳棒为阴极 | |
| B. | 污水中加入适量的硫酸钠,可增强溶液的导电性 | |
| C. | 装置B中通入空气的电极反应是O2+2H2O+4e-=4OH- | |
| D. | 标准状况下,若A装置中产生44.8 L气体,则理论上B装置中要消耗CH411.2L |
2.绿矾(FeSO4•7H2O)是治疗缺铁性贫血药品中的重要成分.下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
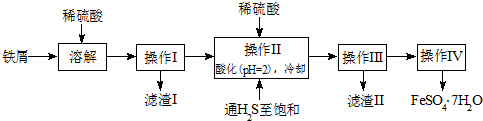
已知:室温下饱和H2S溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5.
请回答下列问题:
(一)绿矾的制备
(1)检验制得的绿矾中是否含有Fe3+的实验操作是取少量溶于水配成溶液,滴加1~2滴KSCN溶液,振荡,若变为红色溶液则含有Fe3+,否则不含Fe3+.
(2)操作II中,通入硫化氢至饱和的目的是把Fe3+还原成Fe2+,除去溶液中的Sn2+,并防止Fe2+被氧化;在溶液中用硫酸酸化至pH=2的目的是防止Fe2+生成沉淀.
(3)操作IV的顺序依次为:蒸发浓缩、冷却结晶、过滤洗涤.
(二)绿矾中FeSO4•7H2O含量的测定
若用容量法测定绿矾中FeSO4•7H2O的含量.滴定反应是:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O
实验方案如下:
①称取15.041g绿矾产品,溶解,在250mL容量瓶中定容.
②量取25.00mL待测溶液于锥形瓶中.
③用0.0500mol/L KMnO4溶液(硫酸酸化)滴定至终点,记录初读数和末读数.
④重复操作②③1~2次或做平行实验1~2次.
⑤数据处理.
(4)上述实验方案中的步骤④是重复操作②③1~2次或做平行实验1~2次.
(5)洁净的滴定管在滴定前必须进行的操作有:
①检验活塞是否漏水;②用蒸馏水洗涤2~3次,再用高锰酸钾标准溶液润洗滴定管2~3次;
③向滴定管中加入KMnO4标准溶液到0刻度以上,赶走尖嘴部位的气泡,调液面至0或0刻度线以下,初读数.
(三)数据处理
某小组同学的实验数据记录如下:(FeSO4•7H2O的摩尔质量为278g/mol)
(6)上述样品中FeSO4•7H2O的质量分数为0.975(用小数表示,保留三位小数).

已知:室温下饱和H2S溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5.
请回答下列问题:
(一)绿矾的制备
(1)检验制得的绿矾中是否含有Fe3+的实验操作是取少量溶于水配成溶液,滴加1~2滴KSCN溶液,振荡,若变为红色溶液则含有Fe3+,否则不含Fe3+.
(2)操作II中,通入硫化氢至饱和的目的是把Fe3+还原成Fe2+,除去溶液中的Sn2+,并防止Fe2+被氧化;在溶液中用硫酸酸化至pH=2的目的是防止Fe2+生成沉淀.
(3)操作IV的顺序依次为:蒸发浓缩、冷却结晶、过滤洗涤.
(二)绿矾中FeSO4•7H2O含量的测定
若用容量法测定绿矾中FeSO4•7H2O的含量.滴定反应是:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O
实验方案如下:
①称取15.041g绿矾产品,溶解,在250mL容量瓶中定容.
②量取25.00mL待测溶液于锥形瓶中.
③用0.0500mol/L KMnO4溶液(硫酸酸化)滴定至终点,记录初读数和末读数.
④重复操作②③1~2次或做平行实验1~2次.
⑤数据处理.
(4)上述实验方案中的步骤④是重复操作②③1~2次或做平行实验1~2次.
(5)洁净的滴定管在滴定前必须进行的操作有:
①检验活塞是否漏水;②用蒸馏水洗涤2~3次,再用高锰酸钾标准溶液润洗滴定管2~3次;
③向滴定管中加入KMnO4标准溶液到0刻度以上,赶走尖嘴部位的气泡,调液面至0或0刻度线以下,初读数.
(三)数据处理
某小组同学的实验数据记录如下:(FeSO4•7H2O的摩尔质量为278g/mol)
| 实验次数 | 初读数(mL) | 末读数(mL) |
| 1 | 0.20 | 21.40 |
| 2 | 0.00 | 21.00 |
| 3 | 1.60 | 26.60 |
9.下列有关说法不正确的是( )
| A. | 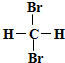 和 和 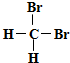 是同一物质 是同一物质 | |
| B. | 1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但它不能解释的事实是邻二溴苯只有一种. | |
| C. | 某有机物化学式为C3H6O2,其核磁共振氢谱有三个峰,其强度比为3:2:1,则该有机物的结构简式一定是CH3CH2COOH | |
| D. | 在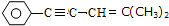 分子中一定共面的碳原子最多为9个,可能共面的碳原子最多为12个 分子中一定共面的碳原子最多为9个,可能共面的碳原子最多为12个 |

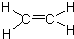 ,C的名称为乙醛
,C的名称为乙醛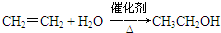 ;反应类型是加成反应;
;反应类型是加成反应;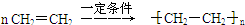 ;反应类型是加聚反应.
;反应类型是加聚反应.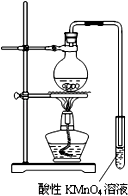 某学习小组探究溴乙烷的消去反应并验证产物.
某学习小组探究溴乙烷的消去反应并验证产物.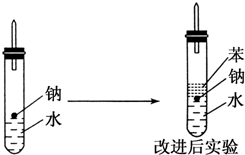 某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:①Zn+盐酸 ②Na+水 ③Al+NaOH溶液.为分析上述三个反应生成的H2,他们设计了如下装置图.
某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:①Zn+盐酸 ②Na+水 ③Al+NaOH溶液.为分析上述三个反应生成的H2,他们设计了如下装置图.