��Ŀ����
14������˵����ȷ���ǣ���������1��3H2��g��+N2��g��?2NH3��g���÷�ӦΪ������Ӧ
��2�����������Ũ�ȣ�һ�����Լӿ�п�����ᷴӦ��ȡ����������
��3�����ڷ�ӦCaCO3��s��?CaO��s��+CO2��g��������CaCO3���������Լӿ�����Ӧ���ʣ�������CaO��CO2��Ũ�ȣ�����Լӿ��淴Ӧ����
��4�����ڷ�Ӧ3H2��g��+N2��g��?2NH3��g�������ܱ������н��У��̶�����������뺤����ѹǿ������ѧ��Ӧ���ʼӿ�
��5�����ڷ�Ӧ3H2��g��+N2��g��?2NH3��g����ʹ�ô��������淴Ӧ����ͬ�ȳ̶ȼӿ죮
| A�� | ��1����2�� | B�� | ��1����2����3�� | C�� | ��1����2����3����4�� | D�� | ��5�� |
���� ��1������������٣�Ϊ�ؼ��ķ�Ӧ��
��2����ΪŨ���ᣬ��п��Ӧ������������
��3�����ӹ��������Ũ�Ȳ��䣻
��4�����뺤�����μӷ�Ӧ�������Ũ�Ȳ��䣻
��5��������ͬ�ȳ̶�����Ӧ���ʣ�
��� �⣺��1���ɷ���ʽ��֪��Ӧ��ļ�����֮�ʹ��������������������٣�Ϊ�ؼ��ķ�Ӧ���ʴ���
��2����ΪŨ���ᣬ��п��Ӧ�������������ʴ���
��3�����ӹ��������Ũ�Ȳ��䣬��Ӧ���ʲ��䣬�ʴ���
��4�����뺤�����μӷ�Ӧ�������Ũ�Ȳ��䣬��Ӧ���ʲ��䣬�ʴ���
��5��������ͬ�ȳ̶�����Ӧ���ʣ����淴Ӧ����ͬ�ȳ̶ȼӿ죮����ȷ��
��ѡD��
���� �����ۺϿ��黯ѧ��Ӧ�������Լ���ѧ��Ӧ���ʵ�Ӱ�죬Ϊ��Ƶ���㣬���ؿ���ѧ���ķ���������ע�������ػ�ѧ��Ӧ���ʵ����أ��ѶȲ���

��ϰ��ϵ�д�
 �����Ծ���ĩ���100��ϵ�д�
�����Ծ���ĩ���100��ϵ�д� ˫��ͬ������ѵ��ϵ�д�
˫��ͬ������ѵ��ϵ�д� �Ƹ�С״Ԫͬ������������ϵ�д�
�Ƹ�С״Ԫͬ������������ϵ�д�
�����Ŀ
1����4mol A�����2mol B������2L �̶�����������л�ϲ���һ�������·������·�Ӧ��2A��g��+B��g��?2C��g��������2s���� C ��Ũ��Ϊ 0.6mol•L-1���������м���˵����������ȷ���ǣ�������
| A�� | ������A��ʾ�ķ�Ӧ��ƽ������Ϊ0.2mol•L-1•s-1 | |
| B�� | ������B��ʾ�ķ�Ӧ��ƽ������Ϊ0.1mol•L-1•s-1 | |
| C�� | 2sʱ����A��ת����Ϊ70% | |
| D�� | 2sʱ����B��Ũ��Ϊ0.7mol•L-1 |
2������˵����ȷ���ǣ�������
| A�� | ����ʵ��ܽʼ��ֻ�е���ʵ��ܽ���̣�û�е���ʵ��������� | |
| B�� | �����ܽ�ﵽƽ��ʱ�����������ʺ��ܽ��������� | |
| C�� | �����ܽ�ﵽƽ��ʱ����Һ�����ʵ�����Ũ����ȣ��ұ��ֲ��� | |
| D�� | �����ܽ�ﵽƽ��ʱ������ټ��������Եĸó�������ٽ��ܽ� |
2�������£����и���������ָ����Һ��һ���ܴ���������ǣ�������
| A�� | 0.1 mol•L-1NaAlO2��Һ��H+��Na+��Cl-��SO42- | |
| B�� | pH=11����Һ�У�CO32-��Na+��AlO2-��NO3-��S2-��SO32- | |
| C�� | ˮ�����H+Ũ��Ϊ10-12mol•L-1����Һ�У�Cl-��CO32-��NO3-��SO32- | |
| D�� | ʹ���ȱ�Ƶ���Һ�У�Fe2+��MnO4-��NO3-��Na+��SO42- |
3��������ʵ��װ����ɶ�Ӧ��ʵ�飨����������ʡ�ԡ����ܴﵽʵ��Ŀ���ǣ���֪HCl��NH3�Ǽ�������ˮ�����壩��������
| A�� | 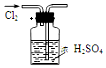 ����Cl2 | B�� |  ����HCl | ||
| C�� |  ������ˮ������ˮ | D�� |  ����NH3 |
 ij����ֻ��C��H��O����Ԫ�أ������ģ����ͼ��ʾ�������й���12��ԭ�ӣ�ͼ��������֮������ߴ���������˫���Ȼ�ѧ������
ij����ֻ��C��H��O����Ԫ�أ������ģ����ͼ��ʾ�������й���12��ԭ�ӣ�ͼ��������֮������ߴ���������˫���Ȼ�ѧ������ ��
��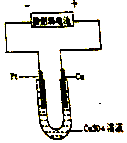 �£�N2H6���ֳ���������һ�ֿ�ȼ�Ե�Һ�壬���������ȼ�ϣ�
�£�N2H6���ֳ���������һ�ֿ�ȼ�Ե�Һ�壬���������ȼ�ϣ�