题目内容
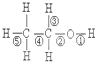 乙醇分子中的化学键如右图所示,在不同反应中断键不同:
乙醇分子中的化学键如右图所示,在不同反应中断键不同:和金属钠反应
考点:乙醇的化学性质
专题:有机物的化学性质及推断
分析:根据乙醇的性质,结合反应物与产物的结构判断.有机反应重在掌握反应的机理即清楚断键与成键位置.
乙醇与与金属钠反应生成乙醇钠和氢气,断开的羟基上的氢氧键;
乙醇在铜催化下与O2反应生成乙醛和水,断开的是羟基上的氢氧键和与羟基所连的碳的氢.
乙醇与与金属钠反应生成乙醇钠和氢气,断开的羟基上的氢氧键;
乙醇在铜催化下与O2反应生成乙醛和水,断开的是羟基上的氢氧键和与羟基所连的碳的氢.
解答:
解:乙醇与金属钠反应生成乙醇钠和氢气:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,故乙醇断键的位置为:①;乙醇在铜催化下与O2反应生成乙醛和水:2CH3CH2OH+O2
2CH3CHO+2H2O,故乙醇断键的位置为①和③,
故答案为:①,2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,①③,2CH3CH2OH+O2
2CH3CHO+2H2O.
| Cu |
| △ |
故答案为:①,2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,①③,2CH3CH2OH+O2
| Cu |
| △ |
点评:本题考查乙醇的性质,难度不大.掌握反应的机理是解题的关键.

练习册系列答案
相关题目
下列离子方程式正确的是( )
| A、醋酸溶解水垢(主要成分是碳酸钙)CaCO3+2H+→CO2↑+Ca2++H2O | ||
| B、高级脂肪酸与氢氧化钠溶液反应:H++OH-=H2O | ||
| C、苯酚钠溶液中通入少量CO2:2C6H5O-+H2O+CO2→2C6H5OH+CO32- | ||
D、乙醛与银氨溶液的反应:CH3CHO+2[Ag(NH3)2]++2OH-
|
汽车尾气(含有烃类、CO、NOx、SO2)是城市空气的主要污染源,治理方法之一是在汽车排气管上加装“催化转化器”,它使CO和NOx反应生成可参与大气生态环境循环的无毒气体,并使烃类充分燃烧及SO2转化,下列说法错误的是( )
| A、CO和NOx反应的化学方程式为:2xCO+2NOx=2xCO2+N2 |
| B、上述方法的缺点是由于CO2增多,会大大提高空气的酸度 |
| C、多植树造林,增大绿化面积,可有效控制城市空气各种污染源 |
| D、汽车改用天然气为燃料或开发氢能源,都会减少对空气的污染 |
实验中的下列操作正确的是( )
| A、把试管中取量过多的Na2CO3溶液又倒入试剂瓶中 |
| B、将含有HNO3的废液倒入水槽中,再用水冲入下水道 |
| C、用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干 |
| D、配制一定物质的量浓度的稀硫酸,浓硫酸溶于水后应冷却至室温才能转移到容量瓶中 |
 硼、碳、硅元素的单质及其化合物的构成自然界的重要物质.请回答下列问题:
硼、碳、硅元素的单质及其化合物的构成自然界的重要物质.请回答下列问题: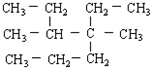 的正确系统命名为
的正确系统命名为