��Ŀ����
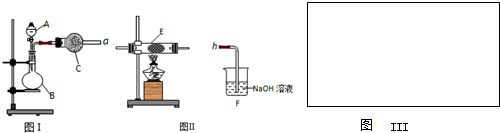
���ù��������Ʊ��������������ʵ��̽������1����0.05mol Na2O2������ƿ�У�����100mL H2O�������ϲ����������ڱ���µ����Ϊ
��2��ȡ����ʵ��õ�����Һ���Թ��У�����2�η�̪��Һ����Һ���ɫ��Ƭ�̺�ɫ��ȥ��
��֪��a����̪��c��OH-��Ϊ1.0��10-4mol/L��2.5mol/Lʱ�ʺ�ɫ������Ϊ��ɫ��
b��H2O2���������ԡ�Ư���ԡ����ȶ��ԣ�
�ټ�ͬѧ��Ϊ����ɫѸ����ȥ����������Һ��c��OH-��������ɵģ���ͨ������Ա����ݼ���˵�������۵��Ƿ���ȷ
����ͬѧ��Ϊ����ɫѸ����ȥ����������Һ�д���H2O2������Դ������Na2O2+2H2O=2NaOH+H2O2������Ƽ�ʵ��֤����ƿ����Һ�к�H2O2������ʵ�������
��������1�����ݷ�Ӧ�ķ���ʽ2Na2O2+2H2O=4NaOH+O2�����㣻
��2�������c��OH-����ȷ����ͬѧ�Ĺ۵��Ƿ���ȷ�������H2O2������������̿�����������
��2�������c��OH-����ȷ����ͬѧ�Ĺ۵��Ƿ���ȷ�������H2O2������������̿�����������
����⣺��1��2Na2O2+2H2O=4NaOH+O2��
2mol 22.4L
0.05mol V
V=
=0.56L��
�ʴ�Ϊ��0.56��
��2������2Na2O2+2H2O=4NaOH+O2����֪����n��NaOH��=0.1mol��c��OH-��=
=1mol/L������1.0��10-4mol/L��2.5mol/L֮�䣬����̪Ϊ��죬���ͬѧ�۵㲻��ȷ��
�ʴ�Ϊ��c��OH-��=1mol/L���ڷ�̪��췶Χ�ڣ�����̪δ��죻
�������H2O2������������̿��������������������壬����ʹľ����ȼ�����ÿ��ö������̼��飬
�ʴ�Ϊ��ȡ������ƿ����Һ���Թ��У�����MnO2�����������壬����ʹľ����ȼ��
2mol 22.4L
0.05mol V
V=
| 0.05mol��22.4L |
| 2mol |
�ʴ�Ϊ��0.56��
��2������2Na2O2+2H2O=4NaOH+O2����֪����n��NaOH��=0.1mol��c��OH-��=
| 0.1mol |
| 0.1L |
�ʴ�Ϊ��c��OH-��=1mol/L���ڷ�̪��췶Χ�ڣ�����̪δ��죻
�������H2O2������������̿��������������������壬����ʹľ����ȼ�����ÿ��ö������̼��飬
�ʴ�Ϊ��ȡ������ƿ����Һ���Թ��У�����MnO2�����������壬����ʹľ����ȼ��
���������⿼���Ƶ���Ҫ�����������ѧ���ķ���������ʵ�������ͼ��������Ŀ��飬Ϊ��Ƶ���㣬ע�����ʵ���ԭ���Ͳ����������ѶȲ���

��ϰ��ϵ�д�
�����Ŀ