题目内容
3.利用Cu和浓硫酸制备SO2的反应涉及的装置,下列说法正确的是( )
| A. | 用装置①制备SO2 | B. | 用装置②检验和收集SO2 | ||
| C. | 用装置③稀释反应后溶液 | D. | 用装置④测定反应后溶液中c(H+) |
分析 A.浓硫酸与铜的反应必须在加热的条件下进行;
B.二氧化硫的密度大于空气,应该采用向上排空气法收集;
C.反应后溶液密度大于水,需要将浓硫酸混合液缓缓加入水中,并用玻璃棒搅拌;
D.氢氧化钠为碱性溶液,应该用碱式滴定管盛放.
解答 解:A.金属Cu与浓硫酸加热反应生成硫酸铜、二氧化硫气体和水,图示装置中缺少加热仪器,无法达到实验目的,故A错误;
B.SO2的密度大于空气,集气瓶中导管应该采用长进短出的方式,图示装置不合理,故B错误;
C.反应后溶液中含有浓硫酸,稀释时将混合液混合倒入烧杯中,同时用玻璃棒不断搅拌,图示操作方法合理,故C正确;
D.NaOH溶液呈碱性,应该用碱式滴定管盛放,图示仪器为酸式滴定管,故D错误;
故选C.
点评 本题考查了化学实验方案的评价,题目难度中等,涉及反应装置选择、气体检验与收集、浓硫酸稀释、滴定管选用等知识,明确常见化学实验基本操作方法为解答关键,试题有利于提高学生的分析能力及化学实验能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.下列关于物质的性质或制备说法正确的是( )
| A. | 用平行光照射氯化钠溶液和氢氧化铁胶体,产生的现象相同 | |
| B. | 铝具有较强的抗腐蚀性质,是因为铝与氧气常温下不反应 | |
| C. | 实验室用MnO2和稀盐酸反应制取氯气 | |
| D. | 工业上用电解熔融氧化铝制取金属铝 |
14.下列各组溶液只用试管和胶头滴管就可以鉴别的是( )
①AlCl3溶液和NaOH溶液
②Ca(HCO3)2溶液和NaOH
③NaAlO2溶液和NaHSO4溶液
④Al2(SO4)3和氨水
⑤AgNO3溶液和氨水.
①AlCl3溶液和NaOH溶液
②Ca(HCO3)2溶液和NaOH
③NaAlO2溶液和NaHSO4溶液
④Al2(SO4)3和氨水
⑤AgNO3溶液和氨水.
| A. | ①③⑤ | B. | ①②③ | C. | ②③④ | D. | ③④⑤ |
11.化学与生产、生活密切相关.下列说法中不正确的是( )
| A. | 使用含有氯化钙的融雪剂会加速桥梁的腐蚀 | |
| B. | 雾霾是一种分散系,N95活性炭口罩可用于防霾,其原理是吸附作用 | |
| C. | 大力推广使用煤的液化、气化技术,能减少二氧化碳的排放 | |
| D. | 晶体硅制得的光电池,能直接将光能转化为电能 |
18.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( )
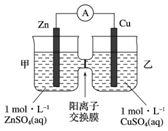

| A. | 锌电极上发生还原反应 | |
| B. | 电池工作一段时间后,甲池的 c(SO42-)不变 | |
| C. | 电池工作一段时间后,乙池溶液的总质量减少 | |
| D. | 阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡 |
3.将一块钠投入到盛有煤油和水的烧杯中,观察到的现象可能是( )
| A. | 钠在水层中反应并四处游动 | |
| B. | 钠停留在煤油层中不发生反应 | |
| C. | 钠在煤油中的液面上反应并四处游动 | |
| D. | 钠在煤油与水的界面处反应并可能上下跳动 |
7.如果你家里有食用植物油和水的混合物,你将采用下列何种方法分离( )
| A. | 过滤 | B. | 蒸馏 | C. | 分液 | D. | 萃取 |
8.下列物质属于能导电的电解质的是( )
| A. | 铜 | B. | 盐酸 | C. | 硫酸 | D. | 熔融的氯化钠 |