题目内容
有反应4HCl+O2→2Cl2+2H2O,已知2molO2被还原时,放出a kJ的热量,且知断开1molO2需要吸收b kJ的热量,断开1molCl2需要吸收c kJ的热量.则断开1mol H-O键比断开1mol H-Cl 键所需能量高( )A.

B.

C.

D.

【答案】分析:设H-Cl键的键能为XkJ/mol,H-O键的键能为YkJ/mol,然后根据反应热=反应物的总键能-生成物的总键能求出H-O键与H-Cl键的键能差;
解答:解:设H-Cl键的键能为XkJ/mol,H-O键的键能为YkJ/mol,因反应热=反应物的总键能-生成物的总键能,所以
-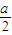 kJ/mol=4XkJ/mol+bkJ/mol-2ckJ/mol-4YkJ/mol,所以Y-X=
kJ/mol=4XkJ/mol+bkJ/mol-2ckJ/mol-4YkJ/mol,所以Y-X=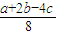 ,即断开1mol H-O键比断开1mol H-Cl 键所需能量高
,即断开1mol H-O键比断开1mol H-Cl 键所需能量高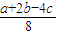 kj.故选:B.
kj.故选:B.
点评:本题主要考查了反应热与键能的关系,掌握反应热=反应物的总键能-生成物的总键能是解题的关键.
解答:解:设H-Cl键的键能为XkJ/mol,H-O键的键能为YkJ/mol,因反应热=反应物的总键能-生成物的总键能,所以
-
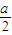 kJ/mol=4XkJ/mol+bkJ/mol-2ckJ/mol-4YkJ/mol,所以Y-X=
kJ/mol=4XkJ/mol+bkJ/mol-2ckJ/mol-4YkJ/mol,所以Y-X=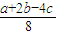 ,即断开1mol H-O键比断开1mol H-Cl 键所需能量高
,即断开1mol H-O键比断开1mol H-Cl 键所需能量高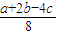 kj.故选:B.
kj.故选:B.点评:本题主要考查了反应热与键能的关系,掌握反应热=反应物的总键能-生成物的总键能是解题的关键.

练习册系列答案
相关题目
有反应4HCl+O2→2Cl2+2H2O,已知2molO2被还原时,放出a kJ的热量,且知断开1molO2需要吸收b kJ的热量,断开1molCl2需要吸收c kJ的热量。则断开1 mol H—O键比断开1 mol H—Cl 键所需能量高
| A.(a+b-2c)/4 | B.(a+2b-4c)/8 | C.(b-a-2c)/4 | D.(2b-a-4c)/8 |