题目内容
某气体在标况下密度为1.25g/L,则其不可能是下面哪种气体( )
| A、CH4 |
| B、CO |
| C、C2H4 |
| D、N2 |
考点:摩尔质量
专题:
分析:根据M=ρVm计算摩尔质量,再利用摩尔质量与相对分子质量的数值相等来解答.
解答:
解:在标准状况下,Vm=22.4L/mol,
由M=ρVm可知,
M=1.25g/L×22.4L/mol=28g/mol,
又摩尔质量与相对分子质量的数值相等,
则该气体的相对分子质量为28,C2H4、CO、N2的摩尔质量都是28g/mol,甲烷摩尔质量为16g/mol,不符合;
故选A.
由M=ρVm可知,
M=1.25g/L×22.4L/mol=28g/mol,
又摩尔质量与相对分子质量的数值相等,
则该气体的相对分子质量为28,C2H4、CO、N2的摩尔质量都是28g/mol,甲烷摩尔质量为16g/mol,不符合;
故选A.
点评:本题考查相对分子质量的计算,明确M=ρVm是解答本题的关键,较简单.

练习册系列答案
相关题目
在一定温度和压强下,2体积X2气体与3体积Y2气体化合生成2体积气体化合物,则该化合物的化学式为( )
| A、XY3 |
| B、XY |
| C、X3Y2 |
| D、X2Y3 |
物质的量相同的甲烷和氨气,一定相等的是( )
| A、体积 | B、质量 |
| C、质子数 | D、原子数 |
下列关于有机物的说法正确的是( )
| A、棉花、羊毛、蚕丝均属于天然纤维素 |
| B、石油的分馏和裂化均属于化学变化 |
| C、油脂都不能使溴的四氯化碳溶液褪色 |
| D、甲烷、乙醇、乙酸在一定条件下都能发生取代反应 |
下列物质属于纯净物的是( )
| A、雾霾 | B、盐酸 | C、碘酒 | D、液氯 |
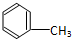 C:CH3CH2OH
C:CH3CH2OH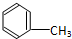 在浓硫酸作用下,与浓硝酸共热至100℃反应的化学方程式为:
在浓硫酸作用下,与浓硝酸共热至100℃反应的化学方程式为: 最近雾霾天气又开始肆虐我国大部分地区.其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2.
最近雾霾天气又开始肆虐我国大部分地区.其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2.