题目内容
某玻璃中含Na2O、CaO、SiO2的质量比约为10:9:58,则此玻璃的组成为
- A.Na2O?CaO?6H2SiO3
- B.Na2O?CaO?6SiO2
- C.2Na2O?2CaO?9SiO2
- D.6Na2O?6CaO?SiO2
B
分析:玻璃的主要成分是硅酸盐,其组成元素可以用元素对应的氧化物来表示,根据氧化物的质量比可以计算元素的原子个数比,进而确定玻璃的组成.
解答:Na2O、CaO、SiO2的质量比约为10:9:58,则Na、Ca、Si的物质的量之比为:(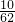 ×2):
×2): :
: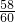 ≈0.32:0.16:0.96=2:1:6,所以氧化物组成为:Na2O?CaO?6SiO2.
≈0.32:0.16:0.96=2:1:6,所以氧化物组成为:Na2O?CaO?6SiO2.
故选B.
点评:玻璃的主要成分是硅酸盐,可以写成氧化物的形式,可以根据元素守恒来确定原子的数目.
分析:玻璃的主要成分是硅酸盐,其组成元素可以用元素对应的氧化物来表示,根据氧化物的质量比可以计算元素的原子个数比,进而确定玻璃的组成.
解答:Na2O、CaO、SiO2的质量比约为10:9:58,则Na、Ca、Si的物质的量之比为:(
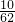 ×2):
×2): :
: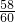 ≈0.32:0.16:0.96=2:1:6,所以氧化物组成为:Na2O?CaO?6SiO2.
≈0.32:0.16:0.96=2:1:6,所以氧化物组成为:Na2O?CaO?6SiO2.故选B.
点评:玻璃的主要成分是硅酸盐,可以写成氧化物的形式,可以根据元素守恒来确定原子的数目.

练习册系列答案
 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目