题目内容
将a g含NaOH样品溶解在bmL0.1mol/L的硫酸中,再加入cmL0.1mol/L的氢氧化钡溶液,反应后所得溶液恰好呈中性,则样品中NaOH的纯度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:化学方程式的有关计算
专题:计算题
分析:发生反应:2NaOH+H2SO4═Na2SO4+2H2O、Ba(OH)2+H2SO4═BaSO4↓+2H2O,反应后所得溶液恰好呈中性,硫酸恰好反应,溶液中溶质为Na2SO4,由方程式可知:n(H2SO4)=
n(NaOH)+n[Ba(OH)2],在根据m=nM计算NaOH的质量,进而计算NaOH质量分数.
| 1 |
| 2 |
解答:
解:发生反应:2NaOH+H2SO4═Na2SO4+2H2O、Ba(OH)2+H2SO4═BaSO4↓+2H2O,反应后所得溶液恰好呈中性,硫酸恰好反应,溶液中溶质为Na2SO4,由方程式可知:n(H2SO4)=
n(NaOH)+n[Ba(OH)2],
则b×10-3 L×0.1mol/L=
n(NaOH)+c×10-3 L×0.1mol/L,
解得n(NaOH)=2(b-c)×10-4mol,
则m(NaOH)=2(b-c)×10-4mol×40g/mol=8(b-c)×10-3g,
故样品中NaOH的纯度是
×100%=
×100%,
故选A.
| 1 |
| 2 |
则b×10-3 L×0.1mol/L=
| 1 |
| 2 |
解得n(NaOH)=2(b-c)×10-4mol,
则m(NaOH)=2(b-c)×10-4mol×40g/mol=8(b-c)×10-3g,
故样品中NaOH的纯度是
| 8(b-c)×10-3g |
| ag |
| (b-c) |
| 125a |
故选A.
点评:本题考查化学方程式的有关计算,比较基础,注意对基础知识的理解掌握.

练习册系列答案
相关题目
一定量的某饱和一元醛(核磁共振氢谱中有三个峰值)发生银镜反应,析出的银为21.6g.等量的此醛完全燃烧时,生成的二氧化碳为8.96L(标准状况),则该醛是( )
| A、乙醛 | B、丙醛 |
| C、丁醛 | D、2-甲基丙醛 |
对如图所示分子的叙述不正确的是( )


| A、能发生碱性水解,1mol该有机物完全反应消耗8mol NaOH |
| B、常温下,与Na2CO3溶液反应放出CO2 |
| C、与稀H2SO4共热,生成两种有机物 |
| D、该有机物的分子式为C14H10O9 |
自来水可以用氯气消毒.某学生用自来水配制下列物质的溶液,不会产生明显药品变质的是( )
| A、石蕊 |
| B、AgNO3 |
| C、NaHCO3 |
| D、FeCl3 |
有机结构理论中有一个重要的观点:有机化合物分子中,原子(团)之间相互影响,从而导致有机化合物化学性质不同.以下事实中,不能够说明此观点的是( )
| A、乙烯能使酸性KMnO4溶液退色,而甲烷不能 |
| B、甲苯能使酸性KMnO4溶液退色,而甲烷不能 |
| C、乙酸能与NaHCO3反应放出气体,而乙醇不能 |
| D、苯硝化反应一般生成硝基苯,而甲苯硝化反应生成三硝基甲苯 |
关于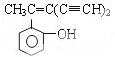 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A、一定在同一平面的碳原子有9个 |
| B、一定在同一平面的碳原子有7个 |
| C、1mol此物质与浓溴水混和最多消耗5mol溴 |
| D、可使KMnO4溶液褪色,是苯酚的同系物 |
下列说法错误的是( )
| A、中国是目前全球最大的稀土生产国和出口国,对稀土元素及其化合物的研究是获得优良催化剂的一种重要途径 |
| B、2013年11月22日,中科院国家纳米科学中心首次“拍”到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键 |
| C、用元素分析仪确定物质中是否含有C、H、O、N、S、Cl、Br等元素,用红外光谱仪确定物质中是否存在某些有机原子团,用原子吸收光谱确定物质中含有哪些金属元素 |
| D、使用可再生资源、用超临界二氧化碳替代有机溶剂、注重原子的经济性、采用低能耗生产工艺符合绿色化学的思想 |
将Mg条投入盛有稀HCl的容器里,产生H2的速率与下列因素:①盐酸浓度 ②温度 ③镁条的表面积 ④容器的密闭情况 ⑤溶液中c(Cl-)大小,有关系的是( )
| A、①② | B、③④ |
| C、①②③④ | D、①②③④⑤ |

