题目内容
将400mL 2mol/L的Na2SO4溶液和100mL 2mol/L Al2(SO4)3的溶液混合,求混合后的溶液中Na+、Al3+、SO42-的物质的量浓度.
考点:物质的量浓度的相关计算
专题:计算题
分析:混合液的体积为400mL+100mL=500mL,先根据n=cV分别计算出硫酸钠、硫酸铝的物质的量,再根据化学式组成计算出Na+、Al3+、SO42-的物质的量,最后根据c=
分别计算出溶液中Na+、Al3+、SO42-的物质的量浓度.
| n |
| V |
解答:
解:两溶液混合后,混合液的体积为400mL+100mL=500mL,
400mL 2mol/L的Na2SO4溶液中含有硫酸钠的物质的量为:n(Na2SO4)=2mol/L×0.4L=0.8mol,
0.8mol中Na2SO4含有钠离子、硫酸根离子的物质的量分别为:n(Na+)=2n(Na2SO4)=0.8mol×2=1.6mol、n(SO42-)=n(Na2SO4)=0.8mol,
100mL 2mol/L Al2(SO4)3的溶液中含有硫酸铝的物质的量为:n(Al2(SO4)3)=2mol/L×0.1L=0.2mol,
0.2mol硫酸铝中含有硫酸根离子、铝离子的物质的量分别为:n(SO42-)=3n(Al2(SO4)3)=0.6mol、n(Al3+)=2n(Al2(SO4)3)=0.4mol,
则混合液中,c(Na+)
=3.2mol/L,c(Al3+)=
=0.8mol/L,c(SO42-)=
=2.8mol/L,
答:混合后的溶液中Na+、Al3+、SO42-的物质的量浓度分别为:3.2mol/L、0.8mol/L、2.8mol/L.
400mL 2mol/L的Na2SO4溶液中含有硫酸钠的物质的量为:n(Na2SO4)=2mol/L×0.4L=0.8mol,
0.8mol中Na2SO4含有钠离子、硫酸根离子的物质的量分别为:n(Na+)=2n(Na2SO4)=0.8mol×2=1.6mol、n(SO42-)=n(Na2SO4)=0.8mol,
100mL 2mol/L Al2(SO4)3的溶液中含有硫酸铝的物质的量为:n(Al2(SO4)3)=2mol/L×0.1L=0.2mol,
0.2mol硫酸铝中含有硫酸根离子、铝离子的物质的量分别为:n(SO42-)=3n(Al2(SO4)3)=0.6mol、n(Al3+)=2n(Al2(SO4)3)=0.4mol,
则混合液中,c(Na+)
| 1.6mol |
| 0.5L |
| 0.4mol |
| 0.5L |
| 0.8mol+0.6mol |
| 0.5L |
答:混合后的溶液中Na+、Al3+、SO42-的物质的量浓度分别为:3.2mol/L、0.8mol/L、2.8mol/L.
点评:本题考查了混合液中物质的量浓度的计算,题目难度不大,注意掌握物质的量浓度的概念及计算方法,本题中需要明确硫酸根离子来自硫酸钠和硫酸铝,为易错点.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
 某物质的晶体中含Ti、O、Ca三种元素,其晶胞排列方式如图所示,晶体中Ti、O、Ca的中原子个数之比为( )
某物质的晶体中含Ti、O、Ca三种元素,其晶胞排列方式如图所示,晶体中Ti、O、Ca的中原子个数之比为( )| A、1:3:1 |
| B、2:3:1 |
| C、2:2:1 |
| D、1:3:3 |
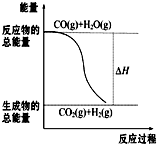 燃烧热是指一定条件下1mol可燃物完全燃烧生成稳定的氧化物时放出的热量.已知热化学方程式:①CO(g)+
燃烧热是指一定条件下1mol可燃物完全燃烧生成稳定的氧化物时放出的热量.已知热化学方程式:①CO(g)+| 1 |
| 2 |
| 1 |
| 2 |
| A、由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41.2 kJ?mol-1 | ||
| B、H2的燃烧热为241.8 kJ?mol-1 | ||
| C、H2(g)转变成H2O(g)的化学反应一定要释放能量 | ||
D、根据②推知反应H2(g)+
|
下列除杂选用的试剂和方法不完全正确的是( )
| 选项 | 被提纯物质 | 杂质 | 试剂 | 方法 |
| A | C2H6 | C2H4 | 溴水 | 洗气 |
| B | C2H4 | SO2 | KMnO4(H+) | 洗气 |
| C | 乙酸乙酯 | 乙酸 | 饱和Na2CO3溶液 | 分液 |
| D | 乙醇 | 水 | CaO | 蒸馏 |
| A、A | B、B | C、C | D、D |
为达到相应的实验目的,下列实验的设计或操作最合理的是( )
| A、为比较Cl与S元素的非金属性强弱,相同条件下,测定相同浓度的NaCl溶液和Na2S溶液的pH值 |
| B、为观察Mg条在CO2气体中的燃烧,在一个集气瓶中收集满CO2气体,取一小段除去表面氧化膜的Mg条用坩埚钳夹持点燃后迅速投入上述集气瓶底部 |
| C、为比较HA和HB两种弱酸的Ka大小,可用pH计测定同温同浓度的NaA溶液和NaB 溶液的pH值 |
| D、为测定一定浓度的NaOH溶液放置空气中是否部分转化为Na2CO3,用甲基橙作指示剂,用标准盐酸溶液滴定 |