题目内容
5.下列四种溶液中,水的电离程度最大的是( )| A. | pH=5的NH4Cl溶液 | B. | pH=5的NaHSO4溶液 | ||
| C. | pH=5盐酸溶液 | D. | pH=8的NaOH溶液 |
分析 溶于水电离出氢离子或氢氧根离子的物质能抑制水电离,含有弱根离子的盐能促进水电离,水溶液中存在离子积常数计算水电离出的离子浓度比较,据此分析解答.
解答 解:A、pH=5的NH4Cl溶液中铵根离子水解,促进水的电离,c(H+)水=10-5mol/L;
B、pH=5的NaHSO4溶液中氢离子抑制水的电离,水电离出的离子浓度c(OH-)水=10-9mol/L;
C、pH=5盐酸溶液抑制水的电离,水电离出离子浓度c(OH-)水=10-9mol/L;
D、pH=8的NaOH溶液中氢氧根离子抑制水的电离,水电离出的离子浓度c(H+)水=10-8mol/L;
综上所述水的电离程度最大的是A;
故选A.
点评 本题考查弱电解质的电离,水的电离平衡也需要因素分析判断,注意硫酸氢钠电离出氢离子导致溶液呈酸性,从而抑制水电离,离子积常数的计算应用是关键,题目较简单.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
15.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,11.2L CCl4所含的分子数为0.5NA | |
| B. | 将含有0.1mol FeCl3的饱和溶液,滴入沸水中加热形成Fe(OH)3胶体,所含的胶体粒子数目少于0.1NA | |
| C. | 1mol/L的氯化钠溶液中,所含离子数为NA | |
| D. | 常温下,CO和N2混合物共2.8g,所含有的原子数为0.1NA |
16.下列晶体熔化时,化学键没有被破坏的是( )
| A. | 氯化钠 | B. | 晶体硅 | C. | 冰 | D. | 烧碱 |
20.纯水不导电,它属于( )
| A. | 强电解质 | B. | 弱电解质 | C. | 非电解质 | D. | 离子化合物 |
10.下列物质在水溶液中的电离方程式错误的是( )
| A. | (NH4)2SO4=2NH4++SO42- | B. | NaHS?Na++HS${\;}^{_}$,HS-=H++S2- | ||
| C. | Ba(OH)2=Ba2++2OH- | D. | HF?H++F- |
15.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,用排水法收集气体 | HX放出的氢气多且反应速率快 | HX酸性比HY强 |
| B | 向2mL 0.1mol/LNa2S溶液中滴2滴0.1mol/LZnSO4溶液;再滴入2滴0.1mol/L CuSO4溶液 | 先生成白色沉淀,后生成黑色沉淀 | 溶度积(Ksp):ZnS>CuS |
| C | 在稀硫酸中加入铜,再加入硝酸钠固体 | 开始无现象,后铜逐步溶解,溶液变蓝,有气泡产生 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 将一铝箔放在酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面生成致密的Al2O3薄膜,且Al2O3熔点高于Al |
| A. | A | B. | B | C. | C | D. | D |
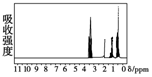


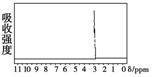
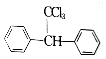 ,其核磁共振氢谱有4组峰,各组吸收峰的面积之比为2:2:2:1.
,其核磁共振氢谱有4组峰,各组吸收峰的面积之比为2:2:2:1.