题目内容
莫尔盐【硫酸亚铁铵(NH4)2SO4?FeSO4?6H2O】是一种重要化学试剂,实验室用含油污的铁片来制取莫尔盐,流程如下:
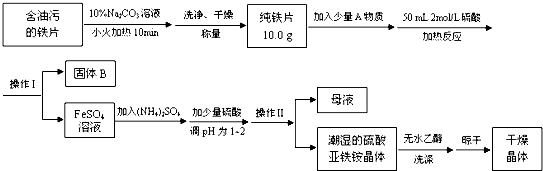
请回答下列问题:
(1)加入10%Na2CO3溶液的原因是 (用离子方程式表示).
(2)A物质可以为 (填编号).
a.CuCl2 b.CuO c.Cu(NO3)2 d.CuSO4
(3)B物质的成分为 .
(4)加少量硫酸调节pH为 1~2的目的是 ,操作Ⅱ的名称 .
(5)用无水乙醇洗涤潮湿的硫酸亚铁铵晶体是为了除去晶体表面残留的水分,不用加热烘干的原因是 .
(6)鉴定所得晶体中含有Fe2+、NH4+、SO42-离子的实验方法正确的是 (填编号).
a.取少量样品于试管,加水溶解,通入适量Cl2,再加KSCN溶液,观察现象
b.取少量样品于试管,加水溶解,加入酸性KMnO4溶液,观察现象
c.取少量样品于试管,加水溶解,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸置于试管口,观察试纸颜色的变化
d.取少量样品于试管,加水溶解,加入盐酸后再加入BaCl2溶液,观察现象.

请回答下列问题:
(1)加入10%Na2CO3溶液的原因是
(2)A物质可以为
a.CuCl2 b.CuO c.Cu(NO3)2 d.CuSO4
(3)B物质的成分为
(4)加少量硫酸调节pH为 1~2的目的是
(5)用无水乙醇洗涤潮湿的硫酸亚铁铵晶体是为了除去晶体表面残留的水分,不用加热烘干的原因是
(6)鉴定所得晶体中含有Fe2+、NH4+、SO42-离子的实验方法正确的是
a.取少量样品于试管,加水溶解,通入适量Cl2,再加KSCN溶液,观察现象
b.取少量样品于试管,加水溶解,加入酸性KMnO4溶液,观察现象
c.取少量样品于试管,加水溶解,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸置于试管口,观察试纸颜色的变化
d.取少量样品于试管,加水溶解,加入盐酸后再加入BaCl2溶液,观察现象.
考点:物质分离和提纯的方法和基本操作综合应用,制备实验方案的设计
专题:实验设计题
分析:(1)碳酸钠水解显碱性,油脂在碱性溶液中完全水解;
(2)A物质为CuO或CuSO4,加入硫酸后和铁发生反应生成铜析出,和铁在硫酸溶液中形成原电池反应加快反应进行;
(3)A物质为CuO或CuSO4,和铁在硫酸溶液中反应,过滤得到固体B为铁和铜;
(4)加入少量硫酸可以调节pH为1~2是抑制亚铁离子和铵根离子水解,得到更多的产品;莫尔盐晶体含有结晶水,蒸干会使晶体分解;
(5)莫尔盐,易溶于水,不溶于乙醇;
(6)Fe2+的检验方法:取少量样品于试管中,加入硫氰酸钾溶液无现象,加入氯水溶液变为血红色或
加入NaOH溶液,先产生白色沉淀,然后变成灰绿色最终变成红褐色;
NH4+的检验方法:取少量样品于试管中,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸置于试管口,试纸变蓝;
SO42-的检验方法:取少量样品于试管,先加入盐酸后无现象,再加入BaCl2溶液,产生白色沉淀;
(2)A物质为CuO或CuSO4,加入硫酸后和铁发生反应生成铜析出,和铁在硫酸溶液中形成原电池反应加快反应进行;
(3)A物质为CuO或CuSO4,和铁在硫酸溶液中反应,过滤得到固体B为铁和铜;
(4)加入少量硫酸可以调节pH为1~2是抑制亚铁离子和铵根离子水解,得到更多的产品;莫尔盐晶体含有结晶水,蒸干会使晶体分解;
(5)莫尔盐,易溶于水,不溶于乙醇;
(6)Fe2+的检验方法:取少量样品于试管中,加入硫氰酸钾溶液无现象,加入氯水溶液变为血红色或
加入NaOH溶液,先产生白色沉淀,然后变成灰绿色最终变成红褐色;
NH4+的检验方法:取少量样品于试管中,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸置于试管口,试纸变蓝;
SO42-的检验方法:取少量样品于试管,先加入盐酸后无现象,再加入BaCl2溶液,产生白色沉淀;
解答:
解:实验室用含油污的铁片来制取莫尔盐:碳酸钠水解显碱性,油脂在碱性溶液中水解生成溶于水的物质易于洗去,步骤1中加入10Na2CO3溶液的主要作用是除去铁屑表面的油污,洗净,干燥,称量得到纯铁片10克,A物质为CuO或CuSO4,加入硫酸后和铁发生反应生成铜析出,和铁在硫酸溶液中形成原电池反应加快反应进行,过滤得到固体B为铁和铜,滤液为FeSO4,相同温度下硫酸亚铁铵晶体在水中的溶解度比硫酸亚铁和硫酸铵的溶解度小,所以将硫酸亚铁和硫酸铵的混合溶液加热浓缩就能得到硫酸亚铁铵晶体,加入少量硫酸可以调节pH为1~2是抑制亚铁离子和铵根离子水解,Fe2++2H2O?Fe (OH)2+2H+; NH4++H2O?NH3?H2O+H+;加入硫酸保持酸性,抑制Fe2+、NH4+离子的水解得到更多的产品;莫尔盐,易溶于水,不溶于乙醇,用乙醇洗涤干燥得到莫尔盐.
(1)油污的主要成分为油脂,在碱性条件下易发生水解,而Na2CO3为强碱弱酸盐,CO32-+H2O?HCO3-+OH-,溶液呈碱性,可用于洗去某些物质表面的油污,
故答案为:CO32-+H2O?HCO3-+OH-;
(2)加入的物质能和铁在硫酸溶液中形成原电池反应加快反应进行,氧化铜不溶于水,A物质为CuO或CuSO4,不引入新的杂质,过滤得到固体为铁和铜;
故答案为:b、d;
(3)氧化铜和硫酸反应生成硫酸铜和水,硫酸铜和铁发生置换反应生成铜和硫酸亚铁,过滤得到固体B为铁和铜;
故答案为:Fe、Cu;
(4)加入少量硫酸可以调节pH为1~2是抑制亚铁离子和铵根离子水解,Fe2++2H2O?Fe (OH)2+2H+; NH4++H2O?NH3?H2O+H+;加入硫酸保持酸性,抑制Fe2+、NH4+离子的水解得到更多的产品;硫酸亚铁铵晶体中的结晶水受热容易失去,所以操作Ⅱ的名称蒸发浓缩、冷却结晶、过滤,
故答案为:抑制Fe2+、NH4+水解;蒸发浓缩、冷却结晶、过滤;
(5)用无水乙醇洗涤晶体,除去其表面的水分,避免加热过程中晶体受热分解(或被氧化),
故答案为:避免加热过程中晶体受热分解(或被氧化);
(6)a.Fe2+的检验方法:取少量样品于试管中,加入硫氰酸钾溶液无现象,加入氯水溶液变为Fe3+,加入硫氰酸钾溶液呈血红色,即Fe3++3SCN-?Fe(SCN)3;取少量样品于试管,加水溶解,通入适量Cl2,如果只存在Fe3+,取少量样品于试管,加水溶解,通入适量Cl2,再加KSCN溶液也呈血红色,故a错误;
b.因为Fe2+具有较强的还原性能使酸性KMnO4溶液褪色,取少量样品于试管,加水溶解,加入酸性KMnO4溶液,观察现象,故b正确;
c.NH4+的检验方法:取少量样品于试管中,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸置于试管口,试纸变蓝,故c正确;
d.SO42-的检验方法:取少量样品于试管,先加入盐酸后无现象,再加入BaCl2溶液,产生白色沉淀,故d正确;
故答案为:b、c、d;
(1)油污的主要成分为油脂,在碱性条件下易发生水解,而Na2CO3为强碱弱酸盐,CO32-+H2O?HCO3-+OH-,溶液呈碱性,可用于洗去某些物质表面的油污,
故答案为:CO32-+H2O?HCO3-+OH-;
(2)加入的物质能和铁在硫酸溶液中形成原电池反应加快反应进行,氧化铜不溶于水,A物质为CuO或CuSO4,不引入新的杂质,过滤得到固体为铁和铜;
故答案为:b、d;
(3)氧化铜和硫酸反应生成硫酸铜和水,硫酸铜和铁发生置换反应生成铜和硫酸亚铁,过滤得到固体B为铁和铜;
故答案为:Fe、Cu;
(4)加入少量硫酸可以调节pH为1~2是抑制亚铁离子和铵根离子水解,Fe2++2H2O?Fe (OH)2+2H+; NH4++H2O?NH3?H2O+H+;加入硫酸保持酸性,抑制Fe2+、NH4+离子的水解得到更多的产品;硫酸亚铁铵晶体中的结晶水受热容易失去,所以操作Ⅱ的名称蒸发浓缩、冷却结晶、过滤,
故答案为:抑制Fe2+、NH4+水解;蒸发浓缩、冷却结晶、过滤;
(5)用无水乙醇洗涤晶体,除去其表面的水分,避免加热过程中晶体受热分解(或被氧化),
故答案为:避免加热过程中晶体受热分解(或被氧化);
(6)a.Fe2+的检验方法:取少量样品于试管中,加入硫氰酸钾溶液无现象,加入氯水溶液变为Fe3+,加入硫氰酸钾溶液呈血红色,即Fe3++3SCN-?Fe(SCN)3;取少量样品于试管,加水溶解,通入适量Cl2,如果只存在Fe3+,取少量样品于试管,加水溶解,通入适量Cl2,再加KSCN溶液也呈血红色,故a错误;
b.因为Fe2+具有较强的还原性能使酸性KMnO4溶液褪色,取少量样品于试管,加水溶解,加入酸性KMnO4溶液,观察现象,故b正确;
c.NH4+的检验方法:取少量样品于试管中,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸置于试管口,试纸变蓝,故c正确;
d.SO42-的检验方法:取少量样品于试管,先加入盐酸后无现象,再加入BaCl2溶液,产生白色沉淀,故d正确;
故答案为:b、c、d;
点评:本题考查了制备硫酸亚铁铵晶体方法,注意合理分析题中信息、掌握物质分离提纯等有关实验操作是解答的关键,注意离子的检验,本题难度中等.

练习册系列答案
相关题目
25℃0.12mol?L-1的NaOH溶液和0.10mol?L-1盐酸等体积混合后,溶液的pH为( )(假设混合后溶液体积可以直接相加)
| A、pH=2 | B、pH=10 |
| C、pH=12 | D、pH=13 |
鉴别苯酚、苯、环己烯、四氯化碳、乙醇、碘化钠溶液,应选用的一种试剂是( )
| A、稀盐酸 |
| B、FeCl3溶液 |
| C、浓溴水 |
| D、酸性高锰酸钾溶液 |
等物质的量浓度的下列五种溶液,①CH3COOH ②(NH4)2CO3③NaHSO4④NaHCO3⑤Ba(OH)2,溶液中水的电离程度由大到小排列正确的是( )
| A、⑤③①④② |
| B、③⑤①②④ |
| C、②④③①⑤ |
| D、②④①③⑤ |
 A、B、C、D、E是中学常见的单质,X是化合物.A、B均为常见的金属,且在地壳中的含量分别为金属元素的前两位;常温下C是气态非金属单质,可以燃烧;D是空气主要成份之一,可与C发生重要工业反应生成X;E是固体非金属单质,在氧气中燃烧时有明亮的蓝紫色火焰.根据上述物质的信息,回答下列有关问题:
A、B、C、D、E是中学常见的单质,X是化合物.A、B均为常见的金属,且在地壳中的含量分别为金属元素的前两位;常温下C是气态非金属单质,可以燃烧;D是空气主要成份之一,可与C发生重要工业反应生成X;E是固体非金属单质,在氧气中燃烧时有明亮的蓝紫色火焰.根据上述物质的信息,回答下列有关问题: 室温下,单质A、B、C分别为铁、黄绿色气体、无色气体,在合适的反应条件下,它们可以按如图所示进行反应.又知E的水溶液是无色的.
室温下,单质A、B、C分别为铁、黄绿色气体、无色气体,在合适的反应条件下,它们可以按如图所示进行反应.又知E的水溶液是无色的. 和
和

