题目内容
25℃、101 kPa时,2g乙醇完全燃烧生成CO2和液态水,同时放出59.4kJ热量,写出该反应的热化学方程式 .
考点:热化学方程式
专题:化学反应中的能量变化
分析:在25℃、101kPa下,2g乙醇燃烧生成CO2和液态水时放热59.4kJ,46g甲醇燃烧生成液态水和二氧化碳气体放热59.4KJ×
=1366.2KJ,依据热化学方程式的书写方法和注意问题,标注对应反应的焓变写出.
| 46 |
| 2 |
解答:
解:在25℃、101kPa下,2g乙醇燃烧生成CO2和液态水时放热59.4kJ,46g甲醇燃烧生成液态水和二氧化碳气体放热59.4KJ×
=1366.2KJ,反应的热化学方程式为:C2H5OH(l)+2O2(g)=2CO2(g)+3H2O(l)△H=-1366.2KJ/mol;
故答案为:C2H5OH(l)+2O2(g)=2CO2(g)+3H2O(l)△H=-1366.2KJ/mol.
| 46 |
| 2 |
故答案为:C2H5OH(l)+2O2(g)=2CO2(g)+3H2O(l)△H=-1366.2KJ/mol.
点评:本题考查了热化学方程式书写方法,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
可逆反应达到平衡的根本原因是( )
| A、反应混合物中各组分的浓度相等 |
| B、正逆反应都还在继续进行 |
| C、正逆反应的速率均为零 |
| D、化学平衡理论是研究怎样使原料尽可能多地转化为产品 |
下列互为同分异构体的一组物质是( )
| A、α-氨基丙酸和硝基丙烷 |
| B、胶棉和火棉 |
| C、苯甲醇和苯酚 |
| D、氨基乙酸和甘氨酸 |

 烯烃分子在一定条件下会发生二分子聚合,其实质是一个分子中饱和碳原子上的一个C-H键断裂,对另一个分子中的双键进行加成.也可以烯烃复分解反应.如:
烯烃分子在一定条件下会发生二分子聚合,其实质是一个分子中饱和碳原子上的一个C-H键断裂,对另一个分子中的双键进行加成.也可以烯烃复分解反应.如:
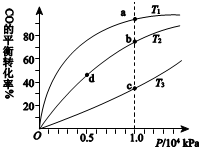 用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)?CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右下图所示.下列说法正确的是( )
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)?CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右下图所示.下列说法正确的是( )