题目内容
实验室需要配制0.2mol?L-1 的Na2CO3溶液250mL,请问:
①需要固体Na2CO3 g;
②需要含结晶水的碳酸钠晶体(Na2CO3?10H2O) g;
③需要物质的量浓度为4mol?L-1的Na2CO3溶液 mL;
④需要溶质的质量分数为12%、密度为1.12g?cm-3的Na2CO3溶液 mL.
①需要固体Na2CO3
②需要含结晶水的碳酸钠晶体(Na2CO3?10H2O)
③需要物质的量浓度为4mol?L-1的Na2CO3溶液
④需要溶质的质量分数为12%、密度为1.12g?cm-3的Na2CO3溶液
考点:溶液的配制
专题:计算题
分析:①根据n=c?V和m=n?M来计算;
②根据1molNa2CO3?10H2O能提供1molNa2CO3,得出需要的Na2CO3?10H2O的物质的量,再根据m=n?M来计算质量;
③根据稀释定律C浓V浓=C稀V稀来计算;
④根据C=
计算出溶液的浓度,然后根据稀释定律C浓V浓=C稀V稀来计算.
②根据1molNa2CO3?10H2O能提供1molNa2CO3,得出需要的Na2CO3?10H2O的物质的量,再根据m=n?M来计算质量;
③根据稀释定律C浓V浓=C稀V稀来计算;
④根据C=
| 1000ρω% |
| M |
解答:
解:①根据n=c?V可知需要的Na2CO3的物质的量n=0.2mol?L-1×0.25L=0.05mol,质量m=n?M=0.05mol×106g/mol=5.3g,故答案为:5.3;
②根据1molNa2CO3?10H2O能提供1molNa2CO3,可知需要的Na2CO3?10H2O的物质的量n=0.05mol,根据m=n?M=0.05mol×286g/mol=14.3g,故答案为:14.3;
③设物质的量浓度为4mol?L-1的Na2CO3溶液Xml,根据稀释定律C浓V浓=C稀V稀可知:4mol/L×Xml×10-3=0.2mol/L×0.25L,解得X=12.5ml,故答案为:12.5;
④根据C=
可知质量分数为12%、密度为1.12g?cm-3的Na2CO3溶液的C=
=1.27mol/L,设需要此Na2CO3溶液的体积为Xml,则根据稀释定律C浓V浓=C稀V稀可知:1.27mol/L×Xml×10-3=0.2mol/L×0.25L,解得X=39.4ml,故答案为:39.4.
②根据1molNa2CO3?10H2O能提供1molNa2CO3,可知需要的Na2CO3?10H2O的物质的量n=0.05mol,根据m=n?M=0.05mol×286g/mol=14.3g,故答案为:14.3;
③设物质的量浓度为4mol?L-1的Na2CO3溶液Xml,根据稀释定律C浓V浓=C稀V稀可知:4mol/L×Xml×10-3=0.2mol/L×0.25L,解得X=12.5ml,故答案为:12.5;
④根据C=
| 1000ρω% |
| M |
| 1000×1.12g/cm3×12% |
| 106g/mol |
点评:本题考查了有关物质的量浓度的计算,掌握好公式的使用方法是解题的关键,难度不大.

练习册系列答案
相关题目
下列叙述中正确的是( )
| A、液态HBr不导电,因此HBr是非电解质 |
| B、强电解质溶液的导电性不一定很强 |
| C、NH3的水溶液能导电,因此NH3是电解质 |
| D、强电解质在液态时一定能导电 |
| E、强电解质在液态时一定能导电 |
氢镍电池的总反应式是H2+2NiO(OH)
2Ni(OH)2.根据此反应判断,下列叙述中不正确的是( )
| 放电 |
| 充电 |
| A、电池放电时,镍元素被氧化 |
| B、电池充电时,氢元素被还原 |
| C、电池放电时,镍元素被还原 |
| D、电池充电时,H2在阴极生成 |
葡萄糖能发生银镜反应是因为它分子结构中含有( )
| A、一OH |
| B、一CHO |
| C、一COOH |
| D、一NH2 |
下列各组物质的二氯代物的同分异构体数目相同的是( )
| A、萘和蒽 |
| B、苯和立方烷 |
| C、金刚烷和四面体烷 |
| D、对二甲苯和丙烷 |
A、B、C、D四种短周期元素的原子半径依次减小,A与C的核电荷数之比为3:4,D能分别与A B C形成电子总数相等的分子X、Y、Z,下列叙述不正确的是( )
| A、X、Y、Z的稳定性逐渐增强 |
| B、A、B、C、D只能形成四种单质 |
| C、X、Y、Z三种化合物的熔沸点逐渐升高 |
| D、只含有A、B、C、D 四种元素的化合物有两种 |
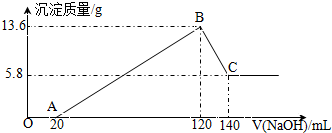 将一定质量的Mg-Al合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应.向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如图.回答下列问题:
将一定质量的Mg-Al合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应.向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如图.回答下列问题: