题目内容
恒温条件下,反应N2(g)+3 H2(g)  2 NH3(g)在密闭容器中达到平衡状态,混合气体的平均摩尔质量为
2 NH3(g)在密闭容器中达到平衡状态,混合气体的平均摩尔质量为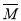 ,N2与NH3的浓度均为c mol/L。若将容器的容积压缩为原来的
,N2与NH3的浓度均为c mol/L。若将容器的容积压缩为原来的 ,当达到新平衡时,下列说法中正确的是( )
,当达到新平衡时,下列说法中正确的是( )
A.新的平衡体系中,N2的浓度小于2 c mol/L大于c mol/L
B.新的平衡体系中,NH3的浓度小于2 c mol/L大于c mol/L
C.新的平衡体系中,混合气体的平均摩尔质量小于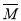
D.新的平衡体系中,气体的密度是原平衡体系的1倍
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、___________、___________。
(2)量取反应物时, 取50 mL 0.50 mol·L-1的盐酸,还需加入的试剂是___________。
取50 mL 0.50 mol·L-1的盐酸,还需加入的试剂是___________。
A.50 mL 0.50 mol·L-1 NaOH溶液 B.50 mL 0.55 mol·L-1 NaOH溶液 C.1.0 g NaOH固体
(3)实验时大烧杯上若不盖硬纸板,求得中和热ΔH的数值 (填偏大、偏小、无影响)。
(4)由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法进行两组测定中和热的实验,实验试剂及其用量如下表所示。
反应物 | 起始温度t1/℃ | 终了温度t2/℃ | 中和热/ kJ·mol-1 |
A.1.0 mol/L HCl溶液50 mL、1.1 mol/L NaOH溶液50 mL | 13.0 | 19.8 ℃ | ΔH1 |
B.1.0 mol/L HCl溶液50 mL、1.1 mol/L NH3·H2O溶液50 mL | 13.0 | 19.3 ℃ | ΔH2 |
① 设充分反应后溶液的比热容c=4.18 J/(g·℃),忽略实验仪器的比热容及溶液体积的变化,则ΔH1= ;ΔH2= 。(已知溶液密度 均为1 g/cm3)
② ΔH1 ≠ ΔH2原因是 。
一定温度下,在三个体积均为1.0 L的恒容密闭容器中,充入一定量的H2和SO2发生下列反应:3 H2(g) + SO2(g) 2 H2O(g) + H2S(g),下列说法正确的是( )
2 H2O(g) + H2S(g),下列说法正确的是( )
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
H2 | SO2 | H2 | SO2 | ||
容器Ⅰ | 300 | 0.3 | 0.1 | 0.02 | |
容器Ⅱ | 300 | 0.6 | 0.2 | ||
容器Ⅲ | 240 | 0.3 | 0.1 | 0.01 | |
A.该反应正反应为吸热反应
B.容器Ⅲ达到平衡的时间比容器I短
C.240℃时,该反应的平衡常数为1.08×104
D.容器Ⅱ达到平衡时SO2的转化率比容器I小


 PCl3(g) + Cl2(g) ② 2 HI(g)
PCl3(g) + Cl2(g) ② 2 HI(g)  O2(g)=SO3(g) ΔH=-315kJ/mol
O2(g)=SO3(g) ΔH=-315kJ/mol O2(g)=H2O(g) ΔH=-241.8kJ/mol
O2(g)=H2O(g) ΔH=-241.8kJ/mol