题目内容
3.25℃、101kP时,甲烷、乙烷和丙烯组成的混合烃32mL,与过量氧气混合并完全燃烧,气体经过浓硫酸干燥,恢复到原来的温度和压强,气体总体积缩小72mL,原混合烃中甲烷、乙烷、丙烯的体积比可能为( )| A. | 3:2:1 | B. | 2:1:2 | C. | 4:2:5 | D. | 1:1:1 |
分析 根据有机物燃烧的化学反应方程式,分析反应前后气体体积的变化,利用气体体积缩小了72mL及混合气体的体积来列等式计算出乙烯的体积,根据计算结果对各选项进行分析.
解答 解:CH4+2O2=CO2+2H2O?△V
1 2 1 2
C2H6+$\frac{7}{2}$O2=2CO2+3H2O△V
1 $\frac{7}{2}$ 2 2.5
C3H6+$\frac{9}{2}$O2=3CO2+3H2O△V
1 $\frac{9}{2}$ 3 2.5
乙烷和丙烯反应后体积缩小的量相同,可将两者看成一种物质,
设乙烷和丙烯一共为xmL,甲烷为ymL,
则:x+y=32、2x+2.5y=72,
解得:x=16,y=16,x:y=16:16=1:1,说明乙烷和丙烯的总体积与甲烷体积相等,
选项中满足条件的只有A,
故选A.
点评 本题考查混合物的计算、根据方程式进行的计算,为高频考点,题目难度中等,侧重于学生的分析能力和计算能力的考查,注意差量法运用简化计算过程.

练习册系列答案
相关题目
将一定量的SO2通入FeCl3溶液中,取混合溶液,分别进行下列实验,能证明SO2与FeCl3溶液发生氧化还原反应的是( )
操作 | 现象 | |
A | 加入NaOH溶液 | 有红褐色沉淀 |
B | 加入Ba(NO3)2溶液 | 有白色沉淀 |
C | 加入酸性KMnO4溶液 | 紫色褪去 |
D | 加入K3[Fe(CN)6](铁氰化钾)溶液 | 有蓝色沉淀 |
11.已知4种短周期元素的离子W3+、X+、Y2-、Z-具有相同的电子层结构,下列判断中正确的是( )
| A. | 原子序数:X>W>Y>Z | B. | 原子半径:W>X>Z>Y | ||
| C. | 氧化性:X+>W3+ | D. | 氢化物稳定性:HZ>H2Y |
7.下列实验装置正确且能达到实验目的是( )
| A. |  提取海带中的碘 | B. |  检验火柴燃烧产生的SO2 | ||
| C. |  测定一定时间内生成H2的反应速率 | D. |  证明非金属性Cl>C>Si |
14.下列化合物在核磁共振氢谱中能出现两组峰.且其峰面积之比不是3:1的有( )
| A. | 均三甲苯 | B. | 丙炔 | C. | 2-甲基丙烯 | D. | 2,3-二甲基丁烷 |
9.1mol乙烯与HCl完全加成后再与Cl2彻底取代,消耗氯气的物质的量是( )
| A. | 2mol | B. | 2.5mol | C. | 4mol | D. | 5mol |
10.判断下列物质按碱性减弱、酸性增强的顺序依次排列正确的是( )
| A. | 厨房清洁剂 肥皂 醋 厕所清洁剂 | |
| B. | 醋 厕所清洁剂 肥皂 厨房清洁剂 | |
| C. | 厕所清洁剂 醋 肥皂 厨房清洁剂 | |
| D. | 厨房清洁剂 厕所清洁剂 醋 肥皂 |
 +3Br2→
+3Br2→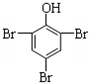 ↓+3HBr;反应类型取代反应.
↓+3HBr;反应类型取代反应. ;反应类型取代反应.
;反应类型取代反应. ;反应类型加聚反应.
;反应类型加聚反应. ;HCN的结构式是H-C≡N;
;HCN的结构式是H-C≡N; ;
; 所含官能团的名称是碳碳双键,醛基;该有机物发生加聚反应后,所得产物的结构简式为
所含官能团的名称是碳碳双键,醛基;该有机物发生加聚反应后,所得产物的结构简式为 .
.