题目内容
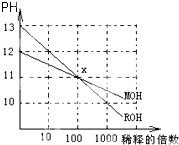 MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示.下列叙述中正确的是( )
MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示.下列叙述中正确的是( )| A、等PH的MOH和ROH溶液,稀释相同倍数,ROH 溶液的PH略大 |
| B、稀释前,c(ROH)=10c(MOH) |
| C、常温下pH之和为14的醋酸和ROH溶液等体积混合,溶液呈碱性 |
| D、在x点,c(M+)=c(R+) |
考点:弱电解质在水溶液中的电离平衡
专题:
分析:由图可知,ROH开始的pH=13,稀释100倍pH=11,则ROH为强碱,而MOH开始的pH=12,稀释100倍pH=11,则MOH为弱碱;并根据酸碱中和及电离来解答.
解答:
解:A.ROH开始的pH=13,稀释100倍pH=11,则ROH为强碱,而MOH开始的pH=12,稀释100倍pH=11,则MOH为弱碱,弱碱稀释时,促进电离,氢氧根离子的物质的量增大,所以等PH的强碱和弱碱,稀释相同的倍数,强碱的pH变化大,则pH相同的MOH和ROH溶液,稀释相同倍数,MOH溶液的PH略大,故A错误;
B.稀释前,c(ROH)=0.1mol/L,c(MOH)>0.01mol/L,则c(ROH)<10c(MOH),故B错误;
C.设醋酸的pH=a,ROH的pH=14-a,则醋酸和ROH溶液等体积混合时V×10-amol/L=V×1014-a-14mol/L,
说明二者溶液中电离出的氢离子和氢氧根离子浓度相等,因醋酸为弱酸,不能完全电离,所以醋酸的浓度大于10-amol/L,醋酸有剩余,溶液显酸性,故C错误;
D.由ROH═R++OH-,MOH?M++OH-可知,在x点,c(OH-)相等,则c(M+)=c(R+),故D正确;
故选D.
B.稀释前,c(ROH)=0.1mol/L,c(MOH)>0.01mol/L,则c(ROH)<10c(MOH),故B错误;
C.设醋酸的pH=a,ROH的pH=14-a,则醋酸和ROH溶液等体积混合时V×10-amol/L=V×1014-a-14mol/L,
说明二者溶液中电离出的氢离子和氢氧根离子浓度相等,因醋酸为弱酸,不能完全电离,所以醋酸的浓度大于10-amol/L,醋酸有剩余,溶液显酸性,故C错误;
D.由ROH═R++OH-,MOH?M++OH-可知,在x点,c(OH-)相等,则c(M+)=c(R+),故D正确;
故选D.
点评:本题考查电解质在水中的电离及图象,明确图象中pH的变化及交点的意义是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
用石墨做电极电解500mLCuSO4溶液.通电一段时间后,测定两极均产生2.24L气体(标准状况下,忽略气体溶解),则CuSO4溶液的物质的量浓度为( )
| A、0.4 mol.L-1 |
| B、0.2 mol.L-1 |
| C、0.3 mol.L-1 |
| D、0.05mol.L-1 |
在醋酸中存在电离平衡:CH3COOH?CH3COO-+H+,要使电离平衡右移且c(H+)增大,应采取的措施是( )
| A、加入NaOH(s) |
| B、加入盐酸 |
| C、加蒸馏水 |
| D、升高温度 |
一定条件下用甲烷可以消除氮氧化物(NOx)的污染.已知:CH4(g)+4NO(g)?2N2(g)+CO2(g)+2H2O(g)△H=-1160.0kJ?mol-1 H2O(l)=H2O(g)△H=+44.0kJ?mol-1 若取一定量的CH4和NO投入到恒容的密闭容器中,下列有关说法正确的是( )
| A、当该反应体系平均分子质量不变时,反应体系达到平衡 |
| B、当容器中每生成1 mol H2O(1)时,放出的能量为536.0kJ |
| C、升高温度,正反应速率加快,平衡常数减小 |
| D、加入高效催化剂可以一定程度上提高NO转化率 |
在下列变化中,需要加入合适的氧化剂才能实现的是( )
| A、Na2O2→O2 |
| B、Cl2→Cl- |
| C、Fe3+→Fe2+ |
| D、Cl-→Cl2 |
下列实验基本操作,主要是出于实验安全考虑的是( )
| A、点燃可燃性气体前验纯 |
| B、气体实验装置在实验前进行气密性检查 |
| C、胶头滴管不能交叉使用 |
| D、实验剩余的药品不能放回原试剂瓶 |
 酒后驾车已成为一个社会问题,2013年1月1日起执行的新交规对酒后驾车作出严厉的处罚规定.检测驾驶人员呼气中酒精浓度(BrAC)的方法有多种.
酒后驾车已成为一个社会问题,2013年1月1日起执行的新交规对酒后驾车作出严厉的处罚规定.检测驾驶人员呼气中酒精浓度(BrAC)的方法有多种.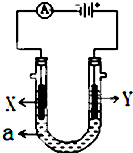 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: