题目内容
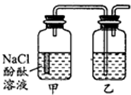 某课外活动小组,将剪下的一块镀锌铁放入试剂瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞溶液,按图装置进行实验,数分钟后观察,下列现象不可能出现的是( )
某课外活动小组,将剪下的一块镀锌铁放入试剂瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞溶液,按图装置进行实验,数分钟后观察,下列现象不可能出现的是( )| A、乙中导气管里形成一段水柱 |
| B、乙中导气管中产生气泡 |
| C、金属片剪口处溶液变红 |
| D、锌被腐蚀 |
考点:实验装置综合
专题:实验题
分析:镀锌铁片,放入锥形瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞试液,形成的原电池中,金属锌为负极,铁为正极,发生吸氧腐蚀,正极反应为2H2O+O2+4e-=4OH-,负极反应为Zn-2e-=Zn2+,结合电极反应解答该题.
解答:
解:A.甲中金属发生吸氧腐蚀,瓶中气体压强减小,导气管里形成一段水柱,故A正确;
B.原电池形成后没有气体生成,所以乙中导气管不会产生气泡,故B错误;
C.正极反应为2H2O+O2+4e-=4OH-,溶液呈碱性,可观察到金属片剪口处溶液变红,故C正确;
D.形成的原电池中,金属锌为负极,发生反应:Zn-2e-=Zn2+,故D正确.
故选B.
B.原电池形成后没有气体生成,所以乙中导气管不会产生气泡,故B错误;
C.正极反应为2H2O+O2+4e-=4OH-,溶液呈碱性,可观察到金属片剪口处溶液变红,故C正确;
D.形成的原电池中,金属锌为负极,发生反应:Zn-2e-=Zn2+,故D正确.
故选B.
点评:本题主要考查了金属的腐蚀,侧重于学生的分析能力的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
标准状况下,m1g气体A与m2g气体B的分子数相等,下列说法中正确的是( )
A、1个A分子的质量是1个B分子的质量的
| ||
B、同温同体积的A与B的质量比为
| ||
C、同温同体积的A与B的分子数比为
| ||
D、同温同压下A与B的密度比为
|
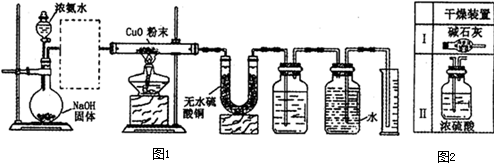
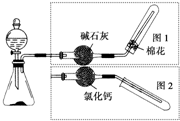 如图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示.下列选项中正确的是( )
如图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示.下列选项中正确的是( )| 发生装置中的药品 | 干燥和集气装置 | |
| A | 铜和稀硝酸 | 图2 |
| B | 氧化钙和浓氨水 | 图2 |
| C | 锌和稀盐酸 | 图1 |
| D | 大理石和稀盐酸 | 图1 |
| A、A | B、B | C、C | D、D |
我国著名化工专家侯德榜先生提出的“侯氏制碱法”大大推进了纯碱工业的发展,他的贡献之一是( )
| A、找到了新型高效催化剂 |
| B、充分利用了能量 |
| C、提高了纯碱产品的纯度 |
| D、有效减少了环境污染 |