题目内容
三草酸合铁酸钾晶体(K3[Fe(C2O4)3]?xH2O)是一种光敏材料,在110℃可完全失去结晶水.为测定该晶体中铁的含量,某实验小组做了如下实验:
Ⅰ.称量5.000g三草酸合铁酸钾晶体,配制成250mL溶液.
Ⅱ.取所配溶液25.00mL于锥形瓶中,加稀硫酸酸化,滴加KMnO4溶液至草酸根(C2O42-)恰好全部氧化成二氧化碳,同时MnO4-被还原成Mn2+.向反应后的溶液中加入一小匙锌粉,加热至溶液的黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性.
Ⅲ.用0.01000mol/L KMnO4溶液滴定步骤Ⅱ所得溶液至终点,消耗KMnO4溶液20.02mL,滴定中MnO4-被还原成Mn2+.
Ⅳ.重复步骤Ⅱ、步骤Ⅲ操作,滴定消耗0.01000mol/L KMnO4溶液19.98mL
请回答下列问题:
(1)配制三草酸合铁酸钾溶液的操作步骤依次是:称量、 、转移、洗涤并转移、 、摇匀.配制过程中的溶液均转移至 (填仪器名称)中.
(2)加入锌粉的目的是 .
(3)写出步骤Ⅲ中发生反应的离子方程式 .
(4)实验测得该晶体中铁的质量分数为 .在步骤Ⅱ中,若加入的KMnO4的溶液的量不够,则测得的铁含量 .(选填“偏低”“偏高”“不变”)
Ⅰ.称量5.000g三草酸合铁酸钾晶体,配制成250mL溶液.
Ⅱ.取所配溶液25.00mL于锥形瓶中,加稀硫酸酸化,滴加KMnO4溶液至草酸根(C2O42-)恰好全部氧化成二氧化碳,同时MnO4-被还原成Mn2+.向反应后的溶液中加入一小匙锌粉,加热至溶液的黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性.
Ⅲ.用0.01000mol/L KMnO4溶液滴定步骤Ⅱ所得溶液至终点,消耗KMnO4溶液20.02mL,滴定中MnO4-被还原成Mn2+.
Ⅳ.重复步骤Ⅱ、步骤Ⅲ操作,滴定消耗0.01000mol/L KMnO4溶液19.98mL
请回答下列问题:
(1)配制三草酸合铁酸钾溶液的操作步骤依次是:称量、
(2)加入锌粉的目的是
(3)写出步骤Ⅲ中发生反应的离子方程式
(4)实验测得该晶体中铁的质量分数为
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:(1)根据配制一定物质的量浓度的溶液的操作步骤判断:在配制物质的量浓度的溶液时,要经过:计算→称量→溶解→移液→洗涤并转移→定容→摇匀等步骤;配制过程中的溶液均转移至250mL容量瓶中;
(2)锌粉能与Fe3+反应,加入锌粉的目的是将Fe3+恰好还原成Fe2+;
(3)根据物质的性质和书写离子方程式的有关要求书写离子方程式;
(4)根据离子方程式计算,n(Fe)=5n(MnO4-)=5×
×0.01 mol?L-1×10-3×10=1.0×10-2mol,m(Fe)=56 g?mol-1×1.0×10-2mol=0.56g.晶体中铁的质量分数=
×100%=11.2%,若在步骤二中滴入酸性高锰酸钾溶液不足,则会有部分草酸根离子未被氧化,在步骤三中则会造成消耗酸性高锰酸钾溶液的量偏大,从而计算出的铁的量增多,含量偏高.
(2)锌粉能与Fe3+反应,加入锌粉的目的是将Fe3+恰好还原成Fe2+;
(3)根据物质的性质和书写离子方程式的有关要求书写离子方程式;
(4)根据离子方程式计算,n(Fe)=5n(MnO4-)=5×
| 20.02mL+19.98mL |
| 2 |
| 0.56g |
| 5g |
解答:
解:(1)在配制物质的量浓度的溶液时,要经过:计算→称量→溶解→移液→洗涤并转移→定容→摇匀等步骤,配制过程中的溶液均转移至250mL容量瓶中,故答案为:溶解;定容;250mL容量瓶;
(2)加入锌粉的目的是将Fe3+恰好还原成Fe2+,故答案为:将Fe3+恰好还原成Fe2+;
(3)在步骤三中发生的离子反应为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,故答案为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
(4)根据步骤三中的离子反应可知:n(Fe)=5n(MnO4-)=5×
×0.01 mol?L-1×10-3×10=1.0×10-2mol,m(Fe)=56 g?mol-1×1.0×10-2mol=0.56g.晶体中铁的质量分数=
×100%=11.2%,若在步骤二中滴入酸性高锰酸钾溶液不足,则会有部分草酸根离子未被氧化,在步骤三中则会造成消耗酸性高锰酸钾溶液的量偏大,从而计算出的铁的量增多,含量偏高.故答案为:11.2%;偏高;
(2)加入锌粉的目的是将Fe3+恰好还原成Fe2+,故答案为:将Fe3+恰好还原成Fe2+;
(3)在步骤三中发生的离子反应为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,故答案为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
(4)根据步骤三中的离子反应可知:n(Fe)=5n(MnO4-)=5×
| 20.02mL+19.98mL |
| 2 |
| 0.56g |
| 5g |
点评:本题考查较为综合,涉及到溶液的配制、滴定和结晶等操作,注意基础实验知识的积累,把握实验步骤、原理和注意事项等问题.

练习册系列答案
相关题目
下列有关热化学方程式的书写及对应的表述均正确的是( )
| A、密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成17.6 g硫化亚铁时,放出19.12 kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6 kJ?mol-1 |
| B、稀醋酸与0.1 mol?L-1 NaOH溶液反应:H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ?mol-1 |
| C、已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式为2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ?mol-1 |
| D、已知2C(s)+O2(g)=2CO(g)△H=-221 kJ?mol-1,则可知C的燃烧热△H=-110.5 kJ?mol-1 |
下列反应的离子方程式书写正确的是( )
| A、硫酸铝溶液中加入过量氨水 Al3++3OH-=Al(OH)3↓ | ||||
B、电解饱和食盐水 2Cl-+2H+
| ||||
| C、在稀氨水中通入过量CO2 NH3?H2O+CO2=NH4++HCO3- | ||||
| D、硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2++2H++H2O2═Fe3++2H2O |
NaCl晶体中钠和氯离子周围都是由六个相反离子按八面体形状排列的,解释这样的结构可以用( )
| A、杂化轨道 | B、键的极性 |
| C、离子大小 | D、离子电荷 |
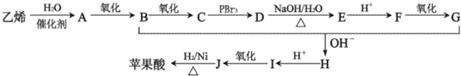
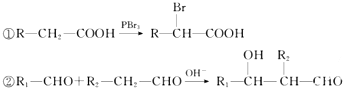
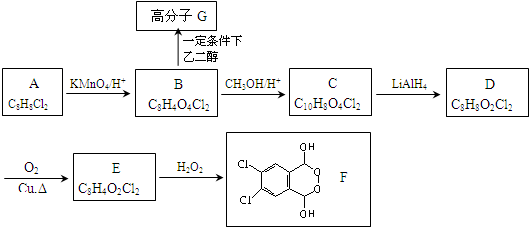
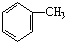

 某烧碱溶液中含有少量杂质(不与盐酸反应),现用标准盐酸滴定NaOH溶液,测定其浓度.
某烧碱溶液中含有少量杂质(不与盐酸反应),现用标准盐酸滴定NaOH溶液,测定其浓度.