��Ŀ����
7����֪1-18��Ԫ�ص�����aW3+��bX+��cY2-��dZ-��������ͬ�ĵ��Ӳ�ṹ���������������ʾ������ȷ���ǣ�������| A�� | ����Ԫ��λ��ͬһ���� | B�� | �⻯����ȶ��ԣ�H2Y��HZ | ||
| C�� | ԭ������a��b��d��c | D�� | a+3=c-2 |
���� 1-18��Ԫ�ص�����aW3+��bX+��cY2-��dZ-��������ͬ�ĵ��Ӳ�ṹ�����Ӿ�Ϊ10����������֪WΪAl��XΪNa��YΪO��ZΪF���Դ������
��� �⣺A��W��Xλ�ڵ������ڣ�Y��Zλ�ڵڶ����ڣ���A����
B���ǽ�����Z��Y�����⻯����ȶ��ԣ�H2Y��HZ����B����
C��W��X��Y��Z��ԭ�������ֱ�Ϊ13��11��8��9����������a��b��d��c����C��ȷ��
D��W��Y��ԭ�������ֱ�Ϊ13��8����a-3=c+2����D����
��ѡC��
���� ���⿼��ԭ�ӽṹ��Ԫ�ص����ʣ�Ϊ��Ƶ���㣬���վ�����ͬ�����Ų�������λ��Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע���Ϊ������Ԫ�أ���Ŀ�ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
17����̼��⼼��������ԭ���ԭ������������ˮ��һ�ֹ��գ�װ����ͼ�����϶˿��ڹرգ��ɵõ�ǿ��ԭ�Ե�H•����ԭ�ӣ������϶˿��ڴ�������������ɵõ�ǿ�����Ե�•OH���ǻ����ɻ���������˵�Ӵ�����ǣ�������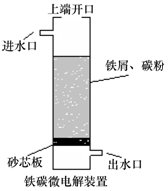

| A�� | �����Ƿ��������������ĵ缫��Ӧʽ��ΪFe-2e-�TFe2+ | |
| B�� | ���������ʱ�������ĵ缫��ӦʽΪH++e-�TH | |
| C�� | �������ʱ��ÿ����1mol•OH��2mol���ӷ���ת�� | |
| D�� | �������в��ᣨH2C2O4������ˮʱ���϶˿���Ӧ��������� |
18�����и�ʽ��ʾˮ�ⷴӦ���ǣ�������
| A�� | HCO3-+H2O?H3O++CO32- | B�� | HS-+H2O?H2S+OH- | ||
| C�� | HSO3-+H2O?SO32-+H3O+ | D�� | HCO3-+OH-?H2O+CO32- |
15����֪CuO������������Cu2O��Cu2O��ϡH2SO4��Ӧ�����ӷ���ʽ��Cu2O+2H+�TCu+Cu2++H2O���ֽ����������պ��CuO��ƷͶ������ϡ�����еõ������Һ���й�˵����ȷ���ǣ�������
| A�� | ��Ӧ��Cu2Oֻ�������� | |
| B�� | ����28.8g Cu2O�μӷ�Ӧ����ת�Ƶ�����Ϊ0.2NA | |
| C�� | Cu2O���ȶ��Ա�CuO�� | |
| D�� | �����Һ�г�����ɫ��˵��CuO�ѷֽ� |
2������˵������ȷ���ǣ�������
| A�� | 12C��14CΪ��ͬ���� | B�� | ʯī��C60��Ϊͬ�������� | ||
| C�� | O2��O3��Ϊͬλ�� | D�� | ${\;}_{17}^{35}$X��${\;}_{17}^{37}$Y Ϊͬ��Ԫ�� |
19�������йػ�ѧ�����ʾ��ȷ���ǣ�������
| A�� | Mgԭ�ӵĽṹʾ��ͼ��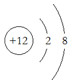 | B�� | OCl2���ӵĵ���ʽ��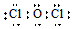 | ||
| C�� | HF���ӵĵ���ʽ��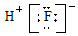 | D�� | Na2S�γɵĵ���ʽ 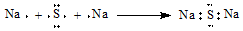 |
16���������ʻ�Ϊͬ���칹���һ���ǣ�������
| A�� | ���ͺ��� | B�� | ����ͱ��� | ||
| C�� | 1H��2H | D�� | CH3CH2OH��CH3OCH3 |
 ��
��