题目内容
8.下列说法中正确的是( )| A. | 氯化钠水溶液在电流的作用下电离出Na+和Cl- | |
| B. | 二氧化碳的水溶液能够导电,故二氧化碳属于电解质 | |
| C. | 碳酸氢钠在水中电离的离子方程式为NaHCO3═Na++H++CO32- | |
| D. | 碳酸钠属于电解质 |
分析 A、电解质的电离不需要通电;
B、二氧化碳的水溶液能导电和二氧化碳本身无关;
C、HCO3-是弱酸的酸式根,在溶液中不能完全电离;
D、在水溶液中或熔融状态下能导电的化合物属于电解质.
解答 解:A、电解质的电离不需要通电,是自发进行的,故A错误;
B、二氧化碳的水溶液能导电和二氧化碳本身无关,是二氧化碳溶于水后生成的碳酸能电离出自由移动的离子而导电,故二氧化碳为非电解质,故B错误;
C、HCO3-是弱酸的酸式根,在溶液中不能完全电离,故碳酸氢钠在水中电离的方程式为NaHCO3═Na++HCO3-,故C错误;
D、在水溶液中或熔融状态下能导电的化合物属于电解质,碳酸钠在水溶液中或熔融状态下能导电,故为电解质,故D正确.
故选D.
点评 本题考查了电离的条件、电解质和非电解质的判断以及电离方程式的书写等问题,难度不大,注意基础的掌握.

练习册系列答案
相关题目
18.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 0.1molCl2含有氯原子数为0.1NA | |
| B. | 标准状况下,22.4LH2O含有的分子数为NA | |
| C. | 3.4gNH3含有的分子数为0.2NA | |
| D. | 0.5mol/L Na2SO3溶液中Na+的物质的量浓度为0.25mol/L |
19.阅读下面短文.
光的散射与丁达尔效应
光通过光学性质不均匀的介质时出现偏离原来传播方向,而沿侧向传播的现象,称为光的散射.在暗室里,将一束经聚集后的光线投射到胶体系统上,在与入射光垂直的方向上,可观察到一条明亮的光路,这就是丁达尔效应.产生丁达尔效应的实质是光的散射.
表1 分散系对可见光的不同作用
当入射光的波长略大于分散相粒子的直径时就发生光的散射.可见光的波长在400~760nm的范围,略大于一般胶体粒子的直径(1~100nm),因此当可见光束投射于胶体时,就发生光的散射,产生丁达尔效应.
对于溶液,分散质分子或离子更小,对可见光的散射作用很微弱;而当可见光束通过浊液时,由于分散质的粒子直径大于入射光的波长,主要发生反射或折射现象.
回答下列问题:
(1)产生丁达尔效应的实质是光的散射.
(2)制备Fe(OH)3胶体,在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入5~6滴饱和的FeCl3溶液,继续煮沸至液体呈红褐色即可.
(3)胶体区别于其他分散系的本质特征是d(填序号).
a.胶体有丁达尔效应 b.胶体粒子可以透过滤纸
c.胶体的胶粒带有电荷 d.胶体粒子的直径在1~100nm之间
(4)CuSO4溶液无明显丁达尔效应的原因是分散质的离子很小,对可见光的散射作用很微弱.
光的散射与丁达尔效应
光通过光学性质不均匀的介质时出现偏离原来传播方向,而沿侧向传播的现象,称为光的散射.在暗室里,将一束经聚集后的光线投射到胶体系统上,在与入射光垂直的方向上,可观察到一条明亮的光路,这就是丁达尔效应.产生丁达尔效应的实质是光的散射.
表1 分散系对可见光的不同作用
| 溶液 | 胶体 | 浊液 | |
| 光路示意图 |  |  |  |
| 对光的主要作用 | 透射 | 散射 | 反射或折射 |
对于溶液,分散质分子或离子更小,对可见光的散射作用很微弱;而当可见光束通过浊液时,由于分散质的粒子直径大于入射光的波长,主要发生反射或折射现象.
回答下列问题:
(1)产生丁达尔效应的实质是光的散射.
(2)制备Fe(OH)3胶体,在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入5~6滴饱和的FeCl3溶液,继续煮沸至液体呈红褐色即可.
(3)胶体区别于其他分散系的本质特征是d(填序号).
a.胶体有丁达尔效应 b.胶体粒子可以透过滤纸
c.胶体的胶粒带有电荷 d.胶体粒子的直径在1~100nm之间
(4)CuSO4溶液无明显丁达尔效应的原因是分散质的离子很小,对可见光的散射作用很微弱.
16.下列物质不是配合物的是( )
| A. | NH4Cl | B. | Fe(SCN)3 | C. | CuSO4•5H2O | D. | [Ag(NH3)2]OH |
3.对溶液、浊液、胶体的下列叙述错误的是( )
| A. | 都呈电中性 | B. | 都是混合物 | ||
| C. | 本质区别是分散质微粒直径大小 | D. | 都能透过滤纸 |
13.下列有机物沸点最高的是( )
| A. | 甲烷 | B. | 乙烷 | C. | 乙醇 | D. | 乙二醇 |
20.1mol如图所示的物质与足量NaOH溶液反应时,消耗NaOH的物质的量最多为( )
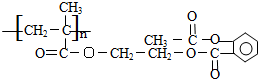
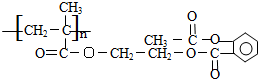
| A. | 3mol | B. | 4mol | C. | 3nmol | D. | 4nmol |
17.有A、B、C、D四种元素的离子A+、B2+、C-、D2-,它们具有相同的电子数,下列判断中,正确的是( )
| A. | A、B、C、D四种元素可能属于同一周期 | |
| B. | A、B、C、D四种元素一定属于短周期元素 | |
| C. | 原子序数由大到小的顺序是B>A>C>D | |
| D. | 离子半径由大到小的顺序是、B2+>A+>C->D2- |
6.下列说法正确的是( )
| A. | 可逆反应的特征是正反应速率和逆反应速率相等 | |
| B. | 在其他条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态 | |
| C. | 在其他条件不变时,升高温度可以使平衡向正反应方向移动 | |
| D. | 对于反应A(g)+3B(g)?2C(g)△H<0达平衡后,温度降低,正反应速率增大,逆反应速率减小,平衡向正反应方向移动 |