题目内容
工业上用铬铁矿(FeO?Cr2O3)冶炼烙的工艺流程如图.

(1)实验室焙烧铬铁矿的仪器名称是 .
(2)操作1名称是 .
(3)工业用某单质在高温下还原Cr2O3冶炼Cr的化学方程式为 .
(4)现有24mL浓度为0.05mol?L-1的Na2SO3溶液恰好与20mL浓度为0.02mol?L-1的Na2Cr2O7溶液完全反应,则Cr元素在产物中的化合价为 .
(5)取FeCl3溶液刻浊铜电路板后的废液,加入一定量铁粉.
①若无固体剩余,则溶液中肯定有的离子是
②若有红色固体,则溶液中肯定没有的离子是
为使废液中FeCl2再生为FeCl3溶液,可向其中加入(填序号)
a.Cl2 b.H2O2 c.浓H2SO4 d.HNO3.

(1)实验室焙烧铬铁矿的仪器名称是
(2)操作1名称是
(3)工业用某单质在高温下还原Cr2O3冶炼Cr的化学方程式为
(4)现有24mL浓度为0.05mol?L-1的Na2SO3溶液恰好与20mL浓度为0.02mol?L-1的Na2Cr2O7溶液完全反应,则Cr元素在产物中的化合价为
(5)取FeCl3溶液刻浊铜电路板后的废液,加入一定量铁粉.
①若无固体剩余,则溶液中肯定有的离子是
②若有红色固体,则溶液中肯定没有的离子是
为使废液中FeCl2再生为FeCl3溶液,可向其中加入(填序号)
a.Cl2 b.H2O2 c.浓H2SO4 d.HNO3.
考点:物质分离和提纯的方法和基本操作综合应用
专题:
分析:铬铁矿中加入纯碱、通入空气焙烧,生成Na2CrO4,过滤后的得到Na2CrO4,加入硫磺,发生氧化还原反应生成Cr(OH)3,灼烧可生成Cr2O3,然后用铝热法冶炼可生成Cr,以此解答该题.
解答:
解:铬铁矿中加入纯碱、通入空气焙烧,生成Na2CrO4,过滤后的得到Na2CrO4,加入硫磺,发生氧化还原反应生成Cr(OH)3,灼烧可生成Cr2O3,然后用铝热法冶炼可生成Cr,
(1)实验室焙烧铬铁矿,应在坩埚中加热,故答案为:坩埚;
(2)经操作1可得到固体和溶液,应为过滤操作,故答案为:过滤;
(3)工业用某单质在高温下还原Cr2O3冶炼Cr,反应的方程式为Cr2O3+2Al
2Cr+Al2O3,故答案为:Cr2O3+2Al
2Cr+Al2O3;
(4)n(Na2SO3)=0.024L×0.05mol?L-1=2.4×10-3mol,n(Na2Cr2O7)=0.02L×0.02mol?L-1=4×10-4mol,
反应后S被氧化为+6价,设Cr被还原为+x价,则2.4×10-3mol×2=4×10-4mol×2×(6-x),
x=3,
故答案为:+3;
(5)FeCl3溶液刻浊铜电路板后的废液中含有Fe3+、Fe2+、Cu2+,加入一定量铁粉,
①若无固体剩余,说明Fe完全反应,且没有Cu生成,则溶液中肯定有的离子Fe2+、Cu2+,故答案为:Fe2+、Cu2+;
②若有红色固体,应铜与Fe3+反应,则溶液中肯定没有的离子,为使废液中FeCl2再生为FeCl3溶液,应加入氧化剂,可加入氯水、过氧化氢,但不能加入硝酸,因引入杂质,则ab正确,故答案为:Fe3+;ab.
(1)实验室焙烧铬铁矿,应在坩埚中加热,故答案为:坩埚;
(2)经操作1可得到固体和溶液,应为过滤操作,故答案为:过滤;
(3)工业用某单质在高温下还原Cr2O3冶炼Cr,反应的方程式为Cr2O3+2Al
| ||
| ||
(4)n(Na2SO3)=0.024L×0.05mol?L-1=2.4×10-3mol,n(Na2Cr2O7)=0.02L×0.02mol?L-1=4×10-4mol,
反应后S被氧化为+6价,设Cr被还原为+x价,则2.4×10-3mol×2=4×10-4mol×2×(6-x),
x=3,
故答案为:+3;
(5)FeCl3溶液刻浊铜电路板后的废液中含有Fe3+、Fe2+、Cu2+,加入一定量铁粉,
①若无固体剩余,说明Fe完全反应,且没有Cu生成,则溶液中肯定有的离子Fe2+、Cu2+,故答案为:Fe2+、Cu2+;
②若有红色固体,应铜与Fe3+反应,则溶液中肯定没有的离子,为使废液中FeCl2再生为FeCl3溶液,应加入氧化剂,可加入氯水、过氧化氢,但不能加入硝酸,因引入杂质,则ab正确,故答案为:Fe3+;ab.
点评:本题以物质的制备流程考查混合物分离提纯的综合应用,为高频考点,涉及流程分析、混合物分离提纯等,把握流程分析及发生的反应为解答的关键,侧重分析与实验能力的考查,综合性较强,题目难度中等.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
阿伏加德罗常数约为6.02×1023mol-1,以下叙述正确的是( )
| A、1mol任何气体单质在标况下体积都约为22.4L,含有的原子数都为2×6.02×1023 |
| B、同温、同压、同体积的氢气和氧气具有相同的分子数 |
| C、在铁与硫的反应中,1mol铁失去的电子数为3×6.02×1023 |
| D、在pH=13 的NaOH 溶液中,OH-的数目为0.1×6.02×1023 |
X、Y、Z均为短周期元素.已知X元素的某种原子核内无中子,Y元素的原子核外最外层电子数是其次外层电子数的2倍,Z元素是地壳中含量最丰富的元素.有下列含该三种元素的化学式:①X2Y2Z2 ②X2Y3Z ③X2YZ2 ④X2Y2Z4⑤X3YZ4 ⑥XYZ3,其中可能存在对应分子的是( )
| A、② | B、②④ |
| C、②⑤⑥ | D、①②③④ |
下列过程属于物理变化的是( )
| A、油脂酸败 | B、空气液化 |
| C、白酒变酸 | D、粉尘爆炸 |
下列实验操作正确的是( )
A、 分离乙醇和水 |
B、 除去氯气中的氯化氢 |
C、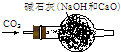 干燥CO2气体 |
D、 读取液体体积 |


