题目内容
15.向氯水中加入下列物质,表中各项均正确的是( )| 选项 | 加入物质 | 现象 | 解释或离子方程式 |
| A | AgNO3溶液 | 有白色沉淀生成 | Cl-+Ag+═AgCl↓ |
| B | 石蕊试液 | 显红色 | 氯水中有盐酸、次氯酸 |
| C | CaCO3 | 有气体放出 | CO32-+2H+═H2O+CO2↑ |
| D | FeCl2和KSCN溶液 | 有红色沉淀生成 | 2Fe2++Cl2═2Fe3++2Cl- |
| A. | A | B. | B | C. | C | D. | D |
分析 A、加入硝酸银有白色沉淀说明溶液中含有氯离子;
B、向氯水中加入石蕊试液,溶液先变红后裉色;
C、碳酸钙是难溶物;
D、硫氰化铁不是沉淀.
解答 解:A、加入硝酸银有白色沉淀说明溶液中含有氯离子,所以反应的离子方程式为:Cl-+Ag+═AgCl↓,故A正确;
B、向氯水中加入石蕊试液,溶液先变红后裉色,说明氯水中有盐酸、次氯酸,故B错误;
C、碳酸钙是难溶物,所以离子反应方程式为:CaCO3+2H+═H2O+CO2↑+Ca2+,故C错误;
D、硫氰化铁不是沉淀,故D错误;
故选A..
点评 本题考查氯水的化学性质,题目难度不大,注意氯水是三分子四离子的微粒,就应具备各微粒的性质.

练习册系列答案
相关题目
5.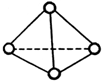 科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图),与白磷分子相似.已知断裂1molN-N键吸收192kJ热量,断裂1molN≡N键吸收946kJ热量,则( )
科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图),与白磷分子相似.已知断裂1molN-N键吸收192kJ热量,断裂1molN≡N键吸收946kJ热量,则( )
 科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图),与白磷分子相似.已知断裂1molN-N键吸收192kJ热量,断裂1molN≡N键吸收946kJ热量,则( )
科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图),与白磷分子相似.已知断裂1molN-N键吸收192kJ热量,断裂1molN≡N键吸收946kJ热量,则( )| A. | 1molN4气体转化为N2时要吸收206kJ能量 | |
| B. | N4是一种新型化合物 | |
| C. | 1molN4气体转化为N2时要放出740kJ能量 | |
| D. | N4是N2的同位素 |
6.判断下列元素中不属于主族元素的是( )
| A. | 钡 | B. | 铅 | C. | 碘 | D. | 铁 |
3.下列化合物中既有离子键又有共价键的是( )
| A. | MgCl2 | B. | NaOH | C. | HBr | D. | N2 |
10.下列有关叙述中正确的是( )
| A. | 溶液中大量共存:Na+、Ba2+、Cl-、CO32- | |
| B. | 无色溶液中能大量共存:NH4+、Fe3+、SO42-、CI- | |
| C. | 氢氧化铁跟硫酸反应的离子方程式是:3H++Fe(OH)3═Fe3++3H2O | |
| D. | 碳酸氢钠溶液跟氢氧化钠反应的离子方程式是:HCO3-+OH-═H2O+CO2↑ |
4. 三氯氢硅(SiHCl3)是生产多晶硅的主要原料.由粗硅制三氯氢硅的反应如下:
三氯氢硅(SiHCl3)是生产多晶硅的主要原料.由粗硅制三氯氢硅的反应如下:
回答下列问题:
(1)写出SiHCl3的结构式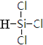 .
.
(z) SiHCl3,在NaOH溶液中剧烈反应放出H2,该反应的化学方程式为SiHCl3+5NaOH=3NaCl+Na2SiO3+H2↑+2H2O.
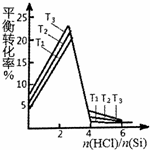
(3)硅的平衡转化率与投料比$\frac{n(HCl)}{n(Si)}$的关系如图,则图中温度T1、T2、T3的大小顺序为T1>T2>T3.
(4)平衡时,$\frac{c(SiHC{l}_{3})}{c(SiC{l}_{4})}$的值a随着$\frac{c({H}_{2})}{c(HCl)}$的值b的变化而变化.则$\frac{a}{b}$=K1/K2(用含Kl、K2的代数式表示);根据关系式,工业上用H2适当稀释HCl来提高SiHCl3的纯度. 请用平衡移动原理加以解释通入H2后两个平衡均逆向移动,但对副反应影响更大,所得产物中副产物
的含量减小,所以SiHCl3的纯度提高.
(5)也可用H2还原SiCl4来制取SiHCl3.300℃时该反应的热化学方程式为H2(g)+SiCl4(g)=SiHCl3(g)+HCl(g)△H=+30kJ•mol-1.
 三氯氢硅(SiHCl3)是生产多晶硅的主要原料.由粗硅制三氯氢硅的反应如下:
三氯氢硅(SiHCl3)是生产多晶硅的主要原料.由粗硅制三氯氢硅的反应如下:| 反应的热化学方程式 | 平衡常数(300℃) | |
| 主反应 | Si(s)+3HCl(g)?SiHCl3(g)+H2(g)△H=-210kJ•mol-1 | K1(mol•L-1)-1 |
| 副反应 | Si(s)+4HCl(g)?SiHCl4(g)+2H2(g)△H=-240kJ•mol-1 | K2(mol•L-1)-1 |
(1)写出SiHCl3的结构式
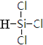 .
.(z) SiHCl3,在NaOH溶液中剧烈反应放出H2,该反应的化学方程式为SiHCl3+5NaOH=3NaCl+Na2SiO3+H2↑+2H2O.
(3)硅的平衡转化率与投料比$\frac{n(HCl)}{n(Si)}$的关系如图,则图中温度T1、T2、T3的大小顺序为T1>T2>T3.
(4)平衡时,$\frac{c(SiHC{l}_{3})}{c(SiC{l}_{4})}$的值a随着$\frac{c({H}_{2})}{c(HCl)}$的值b的变化而变化.则$\frac{a}{b}$=K1/K2(用含Kl、K2的代数式表示);根据关系式,工业上用H2适当稀释HCl来提高SiHCl3的纯度. 请用平衡移动原理加以解释通入H2后两个平衡均逆向移动,但对副反应影响更大,所得产物中副产物
的含量减小,所以SiHCl3的纯度提高.
(5)也可用H2还原SiCl4来制取SiHCl3.300℃时该反应的热化学方程式为H2(g)+SiCl4(g)=SiHCl3(g)+HCl(g)△H=+30kJ•mol-1.