题目内容
在3Cl2+6KOH
KClO3+5KCl+3H2O的反应中,下列说法不正确的是( )
| ||
| A、KCl是还原产物,KClO3是氧化产物 |
| B、Cl2是氧化剂,KOH是还原剂 |
| C、反应中每消耗3 mol Cl2,转移电子数为5NA |
| D、被还原的氯气的物质的量是被氧化的氯气的物质的量的5倍 |
考点:氧化还原反应
专题:
分析:6KOH+3Cl2═KClO3+5KCl+3H2O中,Cl元素的化合价由0升高为+5价,Cl元素的化合价由0降低为-1价,以此来解答.
解答:
解:A.Cl元素的化合价降低被还原,对应的KCl是还原产物,Cl元素的化合价升高被氧化,则KClO3是氧化产物,故A正确;
B.KOH在反应前后各元素的化合价不变,不是还原剂,该反应中只有Cl元素的化合价变化,则氯气既是氧化剂又是还原剂,故B错误;
C.反应中每消耗3mol Cl2,由元素的化合价升高可知,转移1mol×(5-0)=5mol电子,转移电子数为5NA,故C正确;
D.由原子守恒可知,1个Cl原子被氧化,5个Cl原子被还原,则被还原的氯气的物质的量是被氧化的氯气的物质的量的5倍,故D正确;
故选B.
B.KOH在反应前后各元素的化合价不变,不是还原剂,该反应中只有Cl元素的化合价变化,则氯气既是氧化剂又是还原剂,故B错误;
C.反应中每消耗3mol Cl2,由元素的化合价升高可知,转移1mol×(5-0)=5mol电子,转移电子数为5NA,故C正确;
D.由原子守恒可知,1个Cl原子被氧化,5个Cl原子被还原,则被还原的氯气的物质的量是被氧化的氯气的物质的量的5倍,故D正确;
故选B.
点评:本题考查氧化还原反应,把握反应中的元素化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.

练习册系列答案
相关题目
某温度下,在固定容积的容器中,可逆反应A(g)+3B(g)?2C(g)达到平衡,此时测得n(A):n(B):n(C)=2:2:1.若保持温度不变,以n(A):n(B):n(C)=2:2:1的比例向该容器中再充入A B和C则( )
| A、平衡向正反应方向移动 |
| B、平衡向逆反应方向移动 |
| C、平衡不发生移动 |
| D、增大 |
下列说法正确的是( )
| A、6.02×1023个碳原子的质量为1g |
| B、钠原子的摩尔质量为23g |
| C、HCl的摩尔质量等于6.02×1023个HCl分子的质量 |
| D、Na2O2的摩尔质量为78g/mol |
在世界海运史上曾发生过这样一个悲剧:一艘名叫“阿那吉纳号”的货轮满载着精铜砂,在向日本海岸行驶时突然发生大面积漏水,最终沉没.坚硬的钢制船体为什么会突然漏水呢?事后的事故调查结果表明导致沉船的原因与船上的精铜砂密切相关.下列对此调查结论的理解正确的是( )
| A、精铜砂装载过多导致沉船 |
| B、运输途中铜与空气中的氧气发生氧化反应导致质量增大超过船的承载能力 |
| C、在潮湿的环境中,船体与铜构成了原电池,加速了作为负极的船体的腐蚀 |
| D、在潮湿的环境中,船体与铜构成了电解池,钢制船体作阳极而被氧化腐蚀 |
下列不能与溴水发生反应的是( )
①苯 ②乙烯 ③亚硫酸 ④NaOH溶液 ⑤AgNO3溶液 ⑥裂化汽油 ⑦甲烷.
①苯 ②乙烯 ③亚硫酸 ④NaOH溶液 ⑤AgNO3溶液 ⑥裂化汽油 ⑦甲烷.
| A、① | B、①⑦ |
| C、①③⑦ | D、①②⑤⑦ |
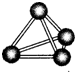 意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如右图所示,下列说正确的是( )
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如右图所示,下列说正确的是( )| A、N4分子属于一种新型的化合物 |
| B、N4分子中只含有非极性键 |
| C、1 mol N4分子所含共价键数为4NA |
| D、N4沸点比P4(白磷)高 |
下列说法正确的是( )
| A、石油干馏可得到汽油、煤油等 |
| B、硫酸铵和醋酸铅溶液均可使鸡蛋清溶液中的蛋白质变性 |
| C、乙醇、乙酸能用碳酸钠溶液、紫色石蕊溶液等多种方法鉴别 |
| D、糖类、蛋白质、脂肪都是重要的营养物质,它们都属于高分子化合物 |
按气流方向,能通过如图装置收集的气体是( )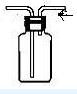

| A、N2 |
| B、NO |
| C、NO2 |
| D、H2 |