题目内容
足量的两份铝粉分别与等体积的盐酸和NaOH 溶液反应,同温同压下产生的气体体积比为1:1,则盐酸和NaOH溶液的物质的量浓度之比为
A.2:3 B.3:1 C.1:2 D.1:1
B
【解析】
试题分析:由2Al+6HCl═2AlCl3+3H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑,可知,参加反应的铝与酸碱与生成的氢气的物质的量关系为:2Al~6HCl~3H2,2Al~2NaOH~3H2,则设在相同条件下产生相同体积的氢气为3mol,需盐酸为6mol,需氢氧化钠为2mol,因盐酸和氢氧化钠溶液的体积相等,根据n=cv,则盐酸和氢氧化钠溶液物质的量浓度之比为6:2=3:1,答案选B。
考点:考查根据化学方程式的计算。

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
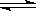 H2+I2
H2+I2