题目内容
9.已知下列物质都可以将盐酸氧化成Cl2,并发生如下还原反应:MnO4-→Mn2+; ClO3-→Cl2; MnO2→Mn2+; ClO-→Cl2;等物质的量的下列化合物与足量浓盐酸反应,得到Cl2的物质的量最少的是( )
| A. | KClO3 | B. | KMnO4 | C. | MnO2 | D. | Ca(ClO)2 |
分析 根据元素化合价的变化判断得失电子的数目,结合反应的方程式解答该题.
解答 解:MnO4-→Mn2+:发生2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O,
ClO3-→Cl2:发生ClO3-+6H++5Cl-=3Cl2↑+3H2O,
MnO2→Mn2+:发生MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
ClO-→Cl2:发生Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O,
假设氧化剂各为1mol,则生成氯气的物质的量分别为2.5mol、3mol、1mol、2mol,
可知得到Cl2的物质的量最少的是MnO2.
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应中基本概念的考查,注意电子数的计算,题目难度不大.

练习册系列答案
相关题目
19.下列叙述正确的是( )
| A. | 氯气的性质活泼,它与氢气混合后立即发生爆炸 | |
| B. | 实验室制取氯气时,为了防止污染,多余氯气用氢氧化钙溶液吸收 | |
| C. | 新制氯水的酸性强于久置氯水 | |
| D. | 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ |
20.下列物质不属于电解质的是( )
| A. | 蔗糖 | B. | H2SO4 | C. | NaOH | D. | NaCl |
17.下列化学反应中,既是置换反应又是氧化还原反应的是( )
| A. | 2Al+6HCl═2 AlCl3+3H2 | B. | 4Na+O2═2Na2O | ||
| C. | MgO+H2SO4═MgSO4+2H2O | D. | Ba(OH)2+H2SO4═BaSO4↓+2H2O |
14.下列关于钠、铝、铁的叙述中正确的是( )
| A. | 都可以与水反应生成氢气和碱 | |
| B. | 都能从硫酸铜溶液中置换出铜 | |
| C. | 去除铝表面的铜镀层可以选用稀硝酸 | |
| D. | 铁丝不论在空气中还是在纯氧中都可以发生氧化还原反应 |
1.下列关于物质用途的说法中,不正确的是( )
| A. | Fe2O3可以做油漆的颜料 | B. | Al2O3可用作耐火材料 | ||
| C. | 王水可以雕刻玻璃 | D. | 赤铁矿可用作炼铁的原料 |
19.下列化学式可表示一个分子的是( )
| A. | SiO2 | B. | NH4Cl | C. | CCl4 | D. | C |
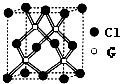 A、B、C、D、E、F、G为原子序数依次增大的前四周期元素.A、F原子的最外层电子数均等于其周期序数.F原子的电子层数是A的3倍; B原子核外电子分处3个不同能级.且每个能级上排布的电子数相同;A与C形成的最简单分子为三角锥形;D原子p轨道上成对电子数等于未成对电子数;E原子核外每个原子轨道上的电子都已成对.E与F同周期;G的原子序数等于A、C、D、F 四种元素原子序数之和.
A、B、C、D、E、F、G为原子序数依次增大的前四周期元素.A、F原子的最外层电子数均等于其周期序数.F原子的电子层数是A的3倍; B原子核外电子分处3个不同能级.且每个能级上排布的电子数相同;A与C形成的最简单分子为三角锥形;D原子p轨道上成对电子数等于未成对电子数;E原子核外每个原子轨道上的电子都已成对.E与F同周期;G的原子序数等于A、C、D、F 四种元素原子序数之和. ;回答E与F原子的第一电离能的大小关系怎样,原因是Mg原子3s能级为全满稳定结构,能量较低;
;回答E与F原子的第一电离能的大小关系怎样,原因是Mg原子3s能级为全满稳定结构,能量较低;