题目内容
用过量铁片与稀盐酸反应,为加快其反应速率而生成氢气的量不变,下列措施中可行的是( )
①以铁屑代替铁片
②用过量锌片代替铁片
③在稀盐酸中加入少量CuSO4溶液
④在稀盐酸中加入CH3COONa固体
⑤在稀盐酸中加入等物质的量浓度的硫酸
⑥在稀盐酸中加入硫酸钾溶液
⑦微热(不考虑HCl的挥发)
⑧在稀盐酸中加入NaNO3固体.
①以铁屑代替铁片
②用过量锌片代替铁片
③在稀盐酸中加入少量CuSO4溶液
④在稀盐酸中加入CH3COONa固体
⑤在稀盐酸中加入等物质的量浓度的硫酸
⑥在稀盐酸中加入硫酸钾溶液
⑦微热(不考虑HCl的挥发)
⑧在稀盐酸中加入NaNO3固体.
| A、除④外 |
| B、除④⑤⑥⑧外 |
| C、除 ④⑥外 |
| D、全部都可行 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:用过量铁片与稀盐酸反应,为加快其反应速率而生成氢气的量不变,则增大接触面积,升高温度,构成原电池等均可加快反应速率,注意可增大氢离子的浓度,但不能增大氢离子的物质的量,以此来解答.
解答:
解:①以铁屑代替铁片,接触面积增大,反应速率加快,故正确;
②用过量锌片代替铁片,Zn比Fe活泼,反应速率加快,故正确;
③在稀盐酸中加入少量CuSO4溶液,Fe置换出Cu,构成原电池,加快反应速率,故正确;
④在稀盐酸中加入CH3COONa固体,氢离子浓度减小,反应速率减小,故错误;
⑤在稀盐酸中加入等物质的量浓度的硫酸,氢离子的物质的量及浓度均增大,反应速率加快,氢气的量增大,故错误;
⑥在稀盐酸中加入硫酸钾溶液,氢离子浓度减小,反应速率减小,故错误;
⑦微热(不考虑HCl的挥发),温度升高,反应速率加快,故正确;
⑧在稀盐酸中加入NaNO3固体,Fe、氢离子、硝酸根离子发生氧化还原反应不生成氢气,故错误;
故选B.
②用过量锌片代替铁片,Zn比Fe活泼,反应速率加快,故正确;
③在稀盐酸中加入少量CuSO4溶液,Fe置换出Cu,构成原电池,加快反应速率,故正确;
④在稀盐酸中加入CH3COONa固体,氢离子浓度减小,反应速率减小,故错误;
⑤在稀盐酸中加入等物质的量浓度的硫酸,氢离子的物质的量及浓度均增大,反应速率加快,氢气的量增大,故错误;
⑥在稀盐酸中加入硫酸钾溶液,氢离子浓度减小,反应速率减小,故错误;
⑦微热(不考虑HCl的挥发),温度升高,反应速率加快,故正确;
⑧在稀盐酸中加入NaNO3固体,Fe、氢离子、硝酸根离子发生氧化还原反应不生成氢气,故错误;
故选B.
点评:本题考查影响化学反应速率的因素,为高频考点,把握常见的外因为解答的关键,注重基础知识的考查,②⑧为解答的易错点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
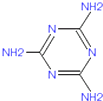 2008年9月,中国爆发三鹿婴幼儿奶粉受污染事件,导致食用了受污染奶粉的婴幼儿产生肾结石病症,其原因是奶粉中含有三聚氰胺.三聚氰胺(英文名Melamine),是一种三嗪类含氮杂环有机化合物,重要的氮杂环有机化工原料.它的结构简式如图,下列说法中不正确的是( )
2008年9月,中国爆发三鹿婴幼儿奶粉受污染事件,导致食用了受污染奶粉的婴幼儿产生肾结石病症,其原因是奶粉中含有三聚氰胺.三聚氰胺(英文名Melamine),是一种三嗪类含氮杂环有机化合物,重要的氮杂环有机化工原料.它的结构简式如图,下列说法中不正确的是( )| A、该物质易溶于热水 |
| B、三聚氰胺的分子式为C3N6H6 |
| C、三聚氰胺属于氨基酸的一种 |
| D、三聚氰胺含氮量很高(66%),因此它能冒充蛋白质 |
以下对于化学键的理解中,正确的是( )
| A、化学键是分子(或晶体)内相邻的两个或多个原子(或离子)之间强烈的作用力 |
| B、化学键存在于任何分子内 |
| C、化学键只存在于离子化合物和共价化合物中 |
| D、氢键和范德华力也是一种化学键 |
在以下的分子或离子中,空间结构的几何形状不是三角锥形的是( )
| A、NF3 |
| B、CH3- |
| C、CO2 |
| D、H3O+ |
 奥运福娃的内充物为无毒的聚酯纤维,其结构简式如图,下列说法正确的是( )
奥运福娃的内充物为无毒的聚酯纤维,其结构简式如图,下列说法正确的是( )| A、羊毛与聚酯纤维的化学成分相同 |
| B、聚酯纤维在强碱溶液中能水解 |
| C、合成聚酯纤维的反应属于加聚反应 |
| D、聚酯纤维可以认为是苯甲酸和乙醇经酯化反应生成 |
 化学概念在逻辑上存在如下关系,下列描述概念间关系的说法正确的是( )
化学概念在逻辑上存在如下关系,下列描述概念间关系的说法正确的是( )| A、化合物与电解质属于交叉关系 |
| B、酸性氧化物与碱性氧化物属于交叉关系 |
| C、分散系与胶体属于包含关系 |
| D、氧化还原反应与化合反应属于并列关系 |
下列离子方程式书写不正确的是( )
| A、碳酸钠溶液中通人少量的CO2:CO32-+CO2+H2O═2HCO3- |
| B、碳酸钙溶于醋酸:CaCO3+2H+═Ca2++H2O+CO2↑ |
| C、CuSO4溶液吸收H2S气体:Cu2++H2S═CuS↓+2H+ |
| D、等体积、等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:Ba2++2OH-+NH4++HCO3-═BaCO3↓+NH3?H2O+H2O |
 某种兴奋剂的结构如图所示,关于它的说法中正确的是( )
某种兴奋剂的结构如图所示,关于它的说法中正确的是( )| A、它的化学式是:C15H18O2NCl |
| B、1mol该物质最多能与2molNaOH反应 |
| C、从结构上看,它属于芳香烃 |
| D、它的分子中所有碳原子共平面 |