题目内容
设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、1 mol AlCl3在熔融状态时离子总数为0.4NA |
| B、标准状况下,2.24L苯中含有的C-H键的数目为0.6NA |
| C、2.2g分子式为 2H218O的水中含有的中子数为1.2 NA |
| D、电解饱和食盐水时,当阴极产生H2 22.4L时,电路中转移的电子数为2NA |
考点:阿伏加德罗常数
专题:
分析:A.氯化铝是共价化合物,熔融状态时不能电离出离子;
B.标准状况下,苯不是气体,无法进行计算;
C.2H218O中含有的中子数为12;
D.外在条件未知.
B.标准状况下,苯不是气体,无法进行计算;
C.2H218O中含有的中子数为12;
D.外在条件未知.
解答:
解:A.氯化铝是共价化合物,熔融状态时不能电离出离子,故A错误;
B.标准状况下,苯不是气体,无法进行计算,故B错误;
C.2.2g 2H218O的物质的量为
=0.1mol,故含有的中子数为0.1×12=1.2mol,即1.2NA,故C正确;
D.外在条件未知,不一定是标况,即22.4L氢气的物质的量不一定是1mol,故D错误,
故选C.
B.标准状况下,苯不是气体,无法进行计算,故B错误;
C.2.2g 2H218O的物质的量为
| 2.2 |
| 22 |
D.外在条件未知,不一定是标况,即22.4L氢气的物质的量不一定是1mol,故D错误,
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,难度中等.注意明确标况下气体摩尔体积的使用条件.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
下列实验操作与安全事故处理正确的是( )
| A、实验剩余的钠可放入废液缸中 |
| B、用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 |
| C、大量氯气泄漏时,迅速离开现场,并逆风前往安全区域疏散 |
| D、不慎洒出的酒精在桌上着火时,立即用大量水扑灭 |
下列说法不符合人与自然和谐相处的是( )
| A、用电动汽车代替燃油汽车 |
| B、将聚乙烯等塑料垃圾深埋或倾入海中 |
| C、用沼气、太阳能、风能等能源替代化石燃料 |
| D、大力实施矿物燃料的脱硫脱硝技术以减少SO2、NOx的排放 |
短周期元素X、Y、Z、W、U原子序数依次递增.X与W位于同一主族,Z元素的单质既能与盐酸反应也能与NaOH溶液反应,W原子的最外层电子数是次外层电子数的一半,Z、W、U原子的最外层电子数之和为13.Y元素的单质在X的某种氧化物中可燃.下列说法正确的是( )
| A、X、W、U的最高价氧化物对应的水化物酸性由强到弱的顺序为:U>W>X |
| B、Y、Z元素的单质作电极,在NaOH溶液中构成原电池,Z电极上产生大量气泡 |
| C、室温下,0.05 mol/L U的气态氢化物的水溶液的pH>1 |
| D、Y、Z、U元素的简单离子半径由大到小的顺序:Y>Z>U |
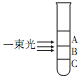 氯化银胶体中的分散质粒子实际上是一个个由很多“AgCl”结合而成的集合体.向盛有NaCl溶液的试管中滴加AgNO3溶液,静置后用一束光照射试管,发现试管的三个不同区域中只有一个区域具有明显的丁达尔效应,则下列分析正确的是( )
氯化银胶体中的分散质粒子实际上是一个个由很多“AgCl”结合而成的集合体.向盛有NaCl溶液的试管中滴加AgNO3溶液,静置后用一束光照射试管,发现试管的三个不同区域中只有一个区域具有明显的丁达尔效应,则下列分析正确的是( )| A、该区域是A,该区域中AgCl的直径最小 |
| B、该区域是B,该区域中AgCl的直径介于A、C区域之间 |
| C、该区域是C,该区域中AgCl的直径最大 |
| D、各区域AgCl的大小都相同,但只有B区域中分散质的大小介于1~100 nm之间 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、32g O3所含有的原子数为2NA |
| B、18g NH4+中所含的离子数为NA |
| C、22.4LCO2所含的原子数为3NA |
| D、1 mol/L碳酸钠溶液中所含钠离子的总数为2 NA |
下列离子方程式中,正确的是( )
| A、明矾净水原理:Al3++3H2O=Al(OH)3↓+3H+ |
| B、向偏铝酸钠溶液中通入少量的CO2气体 AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
| C、向澄清石灰水中滴加盐酸 Ca(OH)2+2H+=Ca2++2H2O |
| D、向碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
已知:O2(g)=O2+(g)+e-△H1=+1175.7kJ?mol-1
PtF6-(g)=PtF6(g)+e-△H2=+771.1kJ?mol-1
O2+(g)+PtF6-(g)=O2PtF6(S)△H3=-482.2kJ?mol-1
则反应O2(g)+PtF6(g)=O2PtF6 (s)的△H是( )
PtF6-(g)=PtF6(g)+e-△H2=+771.1kJ?mol-1
O2+(g)+PtF6-(g)=O2PtF6(S)△H3=-482.2kJ?mol-1
则反应O2(g)+PtF6(g)=O2PtF6 (s)的△H是( )
| A、77.6 kJ |
| B、-77.6 kJ?mol-1 |
| C、+77.6kJ?mol-1 |
| D、-886.8kJ?mol-1 |