题目内容
3.向60mL 18mol•L-1的H2SO4溶液中加入足量的铜片并加热,充分反应后被还原的硫酸的物质的量为( )| A. | 1.08mol | B. | 小于0.54mol | ||
| C. | 在0.54~1.08mol之间 | D. | 大于0.54mol |
分析 发生反应:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,由方程式可知,被还原的硫酸的物质的量是参加反应的硫酸的一半,但随着反应的进行,硫酸的浓度逐渐降低,而铜与稀硫酸并不反应,因此被还原的硫酸的物质的量应小于原硫酸的一半.
解答 解:n(H2SO4)=18mol/L×0.06L=1.08mol,Cu和浓硫酸反应方程式:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,根据方程式知,参加反应的浓硫酸有一半被还原,浓硫酸和Cu反应但稀硫酸和Cu不反应,随着反应的进行,浓硫酸逐渐转化为稀硫酸,所以被还原的浓硫酸小于原硫酸的一半,被还原的硫酸的物质的量小于$\frac{1.08mol}{2}$=0.54mol,
故选:B.
点评 本题考查氧化还原反应的计算、硫酸性质等,明确浓硫酸、稀硫酸性质差异性是解本题关键,很多同学往往认为浓硫酸完全反应而导致错误判断.

练习册系列答案
相关题目
14.下列有关化工生产的说法正确的是( )
| A. | 工业生产硫酸时,常用NaOH吸收尾气中的少量SO2 | |
| B. | 利用Fe3+作为混凝剂,可以对硬水进行软化 | |
| C. | N2与O2作用生成NO,属于氮的固定 | |
| D. | 石油的分馏、煤的气化或液化都是物理变化 |
11.1.68g碳粉与一定量的浓硫酸反应,生成CO2气体2.24L(标况下),则参加该反应的硫酸的物质的量为( )
| A. | 0.2mol | B. | 0.5 mol | C. | 0.56 mol | D. | 0.4 mol |
18.下列关于苯酚的叙述中,正确的是( )
| A. | 苯酚呈弱酸性,能使石蕊试液显浅红色 | |
| B. | 苯酚分子中的13个原子有可能处于同一平面上 | |
| C. | 苯酚可以和硝酸发生加成反应 | |
| D. | 苯酚能与FeCl3溶液反应生成紫色沉淀 |
8.下列事故处理方法正确的是( )
| A. | 汽油失火时,立即用水灭火 | |
| B. | 电线短路失火时,用大量的水灭火 | |
| C. | 浓NaOH 溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 | |
| D. | 浓硫酸溅到皮肤上,立即用稀 NaOH 溶液洗涤 |
15.有a、b、c、d四个金属电极,G为电流计.有关的反应装置及部分反应现象如下:
由此可判断这四种金属的活动性顺序是( )
| 实验 装置 | 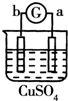 | 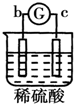 | 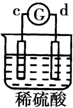 | 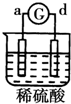 |
| 部分实验现象 | a极质量减小b极质量增加 | 溶液中的SO42-向b极移动 | d极溶解c极有气体产生 | 电子从d极流向 a极 |
| A. | d>a>b>c | B. | a>b>c>d | C. | b>c>d>a | D. | a>b>d>c |
12.下列说法不正确的是( )
| A. | 通过煤的干馏可以获得焦炭 | |
| B. | 煤中含有苯和甲苯,可以用蒸馏的方法把它们分离出来 | |
| C. | 石油裂解的目的是为了得到乙烯、丙烯和1,3-丁二烯等短链不饱和烃 | |
| D. | 煤液化后可以得到甲醇 |

 )与新制氢氧化铜反应的化学方程式C6H5CHO+NaOH+2Cu(OH)2$\stackrel{水浴}{→}$C6H5COONa+Cu2O↓+3H2O
)与新制氢氧化铜反应的化学方程式C6H5CHO+NaOH+2Cu(OH)2$\stackrel{水浴}{→}$C6H5COONa+Cu2O↓+3H2O