题目内容
4.已知在容积固定的密闭容器中充入NH3和O2发生如下反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)(1)下列能说明该反应已经达到平衡状态的是BDE;
A.容器中气体总质量不变 B.c(O2)不变C.υ(O2)=1.25υ(NH3) D.体系压强不变
E.相同时间内,消耗0.1mol NH3,同时消耗了0.1mol NO
(2)向该容器中加入正催化剂,则反应速率增大(填“增大”、“减小”或“不变”,下同),降低容器的温度则反应速率减小,通入Ar,则反应速率不变 .
(3)若反应在绝热密闭系统中进行时,其余条件不变,反应速率是先增大后减小,其原因是反应放热反应速率加快,随着反应的进行反应物浓度减小,反应速率减小.
分析 (1)根据化学平衡状态的特征:逆、定、动、变、等来判断化学反应是否达到平衡;当化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再发生变化,由此衍生的一些物理性不变,以此解答该题;
(2)催化剂能够加快反应速率,降温反应速率减慢,容器体积不变时通入稀有气体反应速率不变;
(3)根据该反应为放热反应,反应过程中温度升高,此条件下比原平衡温度高进行分析反应速率变化;随后浓度变化成为影响反应速率的主要因素.
解答 解:(1)A.反应前后都是气体,气体质量始终不变,故A错误;
B.c (O2)不变,说明正逆反应速率相等,达到了平衡状态,故B正确;
C.v(O2)=1.25v(NH3),没有告诉是正逆反应速率,无法判断是否达到平衡状态,故C错误;
D.该反应是体积缩小的反应,反应过程中气体的物质的量逐渐减小,压强逐渐减小,若体系压强不变,说明正逆反应速率相等,达到了平衡状态,故D正确;
E.相同时间内,消耗0.1mol NH3,同时消耗了0.1mol NO,说明正逆反应速率相等,反应达到平衡状态,故E正确;
故答案为:BDE;
(2)在容器中加入正催化剂,正反应速率和逆反应速率都增大,平衡不发生移动;降低温度,正逆反应速率同时减小,容器体积不变充入Ar,各组分浓度不变,反应速率不变,
故答案为:增大;减小;不变;
(3)由于该反应为放热反应,若在容积固定的绝热密闭容器中发生上述反应,其余条件不变,反应过程中反应体系的温度高于原反应,所以正逆反应速率都增大,随后因浓度减小成为影响的主要因素,所以反应减慢,
故答案为:反应放热反应速率加快,随着反应的进行反应物浓度减小,反应速率减小.
点评 本题考查了化学平衡状态的判断、化学平衡的影响因素、影响化学反应速率的因素,题目难度中等,注意掌握判断化学平衡状态的方法,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案| A. | 标准状况下,22.4LNO与11.2LO2混合,混合气体所含分子数为NA | |
| B. | 1molAl3+含有的核外电子数为10NA | |
| C. | 常温常压下,1mol氮气含有的原子总数为2NA | |
| D. | 1L1mol/LFeCl3溶液全部制成胶体,其中含胶粒的数目小于NA |
| A. | 滴加盐酸时,HCl是还原剂,Cl2是还原产物 | |
| B. | 已知Bi为第ⅤA族元素,上述实验说明Bi具有较强的非金属性 | |
| C. | 若有0.1 mol NaBiO3参加了反应,则整个过程转移电子0.4NA | |
| D. | 此实验条件下,物质的氧化性:KMnO4>NaBiO3>Cl2 |
| A. | 位于短周期的X元素的阳离子与Y元素的阴离子具有相同的电子层结构,则两元素的原子序数一定是X<Y | |
| B. | 共价化合物的熔沸点都比较低 | |
| C. | 热稳定性:AsH3<PH3<H2O<HF | |
| D. | 最外层电子数较少的金属元素,不一定比最外层电子数较多的金属元素活泼性强 |
Hg(l)+$\frac{1}{2}$O2(g)=HgO(s);△H=-90.7kJ/mol,
由此可知反应:Zn(s)+HgO(s)=ZnO(s)+Hg(l)的△H为( )
| A. | △H=-1141.8kJ/mol | B. | △H=+260.4kJ/mol | ||
| C. | △H=+441.8kJ/mol | D. | △H=-260.4kJ/mol |
| A. | 18g H2O在标准状况下的体积是22.4L | |
| B. | 常温常压下,4g H2含有的分子数为 2NA | |
| C. | 2.3g金属钠变为钠离子时失去的电子数为NA | |
| D. | 17g氨气所含原子数目为3NA |
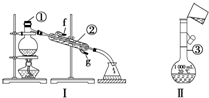 掌握仪器的名称及使用方法是化学实验的基础,如图所示为两套实验装置.
掌握仪器的名称及使用方法是化学实验的基础,如图所示为两套实验装置.