题目内容
7.某学习小组在通过反应Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O研究反应速率的影响因素后,对Na2S2O3产生了兴趣,查资料知Na2S2O3名称为硫代硫酸钠,俗称海波,可以看成是用一个S原子取代了Na2SO4中的一个O原子而形成.该实验小组运用类比学习的思想预测了Na2S2O3的某些性质,并通过实验探究验证自己的预测.[提出假设]
(1)部分学生认为Na2S2O3与Na2SO4结构相似,化学性质也相似,因此室温时Na2S2O3溶液的pH=7(填“>”、“=”或“<”)
(2)部分学生从S元素化合价推测Na2S2O3与SO2性质相似,均具有较强的还原性.
[实验探究]
取适量Na2S2O3晶体,溶于水中制成Na2S2O3溶液,进行如下探究(填写下表中空格).
| 实验操作 | 实验现象 | 现象解释(用离子方程式表示) | |
| 探究① | (3)用玻璃棒蘸取Na2S2O3溶液点在pH试纸中部,将试纸颜色与标准比色卡对照 | 溶液PH=8 | (4)S2O32-+H2O?HS2O3-+OH- |
| 探究② | 向新制氯水(PH<2)中滴加少量Na2S2O3溶液 | 氯水颜色变浅 | (5)Na2S2O3具有还原性 |
(6)探究①:硫代硫酸钠水溶液呈碱性.
(7)探究②:硫代硫酸钠具有还原性.
[问题讨论]
(8)甲同学向“探究②”反应后的溶液中滴加硝酸银溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化.你认为该方案是否正确并说明理由该方案不合理,因氯水过量,Ag+ 与Cl- 会生成AgCl沉淀.
(9)请你重新设计一个实验方案,证明Na2S2O3被氯水氧化.你的方案是取反应后的溶液少量,加入氯化钡溶液,再加入盐酸,若产生的沉淀不溶解,则硫代硫酸钠被氧化了,否则没被氧化.
分析 提出假设:(1)Na2S2O3与Na2SO4结构相似,化学性质也相似,则Na2S2O3溶液呈中性;
(2)Na2S2O3、SO2中S元素化合价均为+4价,具有较强的还原性;
实验探究与实验结论:探究①.用pH试纸沉淀溶液pH,Na2S2O3溶液呈碱性,说明S2O32-水解;
探究②.氯水颜色变浅,说明硫代硫酸钠把Cl2还原;
问题讨论:(8)氯水过量,溶液中含有氯离子;
(9)检验溶液中是否有硫酸根离子,说明硫代硫酸钠被氯气氧化.
解答 解:(1)Na2S2O3与Na2SO4结构相似,化学性质也相似,则Na2S2O3溶液呈中性,室温时Na2S2O3溶液的pH=7,
故答案为:=;
(2)Na2S2O3、SO2中S元素化合价均为+4价,具有较强的还原性,
故答案为:还原性;
(3)实验探究①的目的是测定溶液的pH,方法为用玻璃棒蘸取Na2S2O3溶液点在pH试纸中部,将试纸颜色与标准比色卡对照,
故答案为:用玻璃棒蘸取Na2S2O3溶液点在pH试纸中部,将试纸颜色与标准比色卡对照;
(4)测定溶液pH=8说明溶液呈碱性,证明硫代硫酸跟离子水解显碱性,反应的离子方程式为:S2O32-+H2O?HS2O3-+OH-,
故答案为:S2O32-+H2O?HS2O3-+OH-;
(5)向新制氯水(pH<2)中滴加少量Na2S2O3溶液,氯水和硫代硫酸钠反应氯水褪色变浅,说明氯气发生反应表现氧化性把硫代硫酸钠氧化为硫酸钠,反应的离子方程式为:S2O32-+4Cl2+5H2O═2SO42-+8Cl-+10H+,
故答案为:S2O32-+4Cl2+5H2O═2SO42-+8Cl-+10H+;
(6)依据探究①是硫代硫酸钠溶液pH=8,硫代硫酸钠水溶液呈碱性,
故答案为:硫代硫酸钠水溶液呈碱性;
(7)向新制氯水(pH<2)中滴加少量Na2S2O3溶液,氯水和硫代硫酸钠反应氯水褪色变浅,说明硫代硫酸钠把Cl2还原,氯气发生反应表现氧化性,把硫代硫酸钠氧化为硫酸钠,证明Na2S2O3具有还原性,
故答案为:硫代硫酸钠具有还原性,
(8)探究②是向新制氯水(pH<2)中滴加少量Na2S2O3溶液,氯水过量溶液中一定有氯离子,Ag+ 与Cl- 会生成AgCl沉淀,所以方案不正确;
故答案为:该方案不合理,因氯水过量,Ag+ 与Cl- 会生成AgCl沉淀;
(9)证明Na2S2O3被氯水氧化,可以利用硫代硫酸钠被氯气氧化生成的硫酸根离子检验,检验方法为:取反应后的溶液少量,加入氯化钡溶液,再加入盐酸,若产生的沉淀不溶解,则硫代硫酸钠被氧化了,否则没被氧化,
故答案为:取反应后的溶液少量,加入氯化钡溶液,再加入盐酸,若产生的沉淀不溶解,则硫代硫酸钠被氧化了,否则没被氧化.
点评 本题考查物质性质的探究实验,注意掌握探究实验的一般步骤,是对学生综合能力的考查,题目难度中等.

| A. | 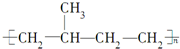 | B. | 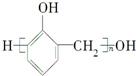 | ||
| C. | 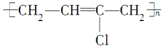 | D. | 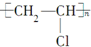 |
| A. | 75%的酒精溶液 | B. | 硝酸钠 | C. | 碱石灰 | D. | 豆浆 | ||||
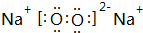
| E. | 过氧化钠 |
| A. | X、Y、W的最高价含氧酸酸性顺序:Y>W>X | |
| B. | 气态氢化物的稳定性:Z<W | |
| C. | X、W形成的化合物XW4属于离子化合物 | |
| D. | 原子半径:Z>W>X>Y |
| A. | 该反应中Fe2+是还原剂,O2是还原产物 | |
| B. | 该反应中Na2O2仅作氧化剂 | |
| C. | 4molNa2O2在反应中共得到8NA个电子 | |
| D. | Fe(OH)3是氧化产物,每生成1molO2反应过程中共转移6mol电子 |
 .
.