��Ŀ����
3��ij�о�С����֤�Ҵ��Ļ�ԭ�ԣ�װ����ͼ1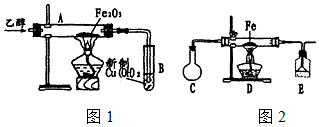
��1���Ҵ��������IJ���Ϊ��ȩ��1mol�Ҵ�ʧȥ2mol���ӣ�
��2��ͨ���Ҵ���Ӧ���Թ�A�������Ǻ�ɫ�����ڣ���Ӧ������������Թ�B���м��ȣ�������ֵ�������ש��ɫ������
��3���о�С�鷢�֣���Ӧ�����в�����ˮ��������֣��ռ�������֤����H2��Ϊ�˽�һ���о��������ͼ2�ã����ּ���������ʡ�ԣ���
��Cװ��ʢ�е��������Ҵ����ȼ���C����װ�ô��ţ�������װ���ڵĿ�����
��E�ռ�Һ��������Ϊ�����ᣬ����Ϊ������ȩ�������ж�˭���Ʋ����������˵�����ɣ�����ȷ��������Ԫ���غ�͵�ʧ���ӣ��������������������������������ϩ������ʵ����������������ȷ��
���� ��1���Ҵ����л�ԭ�ԣ�������������ȩ������C2H6O��C2H4O��Ԫ�ػ��ϼ۱仯�ж�ת�Ƶ�������
��2���Ҵ����л�ԭ�ԣ��ܻ�ԭ������������������������Ϊ��ȩ����ȩ�ܹ�������������ͭ�����������ᣬ������ͭ����ԭΪ������ͭ��������ʵ���ɫ���
��3���������Ҵ������ǻ��ܹ��������Ӧ�����������²�C����Ϊ�Ҵ���Ϊ��ֹ����������������Ӧ��Ӧ�����Ҵ������ų�װ���ڿ�����
�����������غ��������ԭ��Ӧ��ʧ�����غ��жϽ��
��� �⣺��1���Ҵ����л�ԭ�ԣ�������������ȩ��C2H6O��̼Ԫ��Ϊ-2�ۣ�C2H4O��̼Ԫ��Ϊ-1�ۣ�������1mol�Ҵ�ʧȥ2mol���ӣ�
�ʴ�Ϊ����ȩ�� 2��
��2���Ҵ����л�ԭ�ԣ��ܻ�ԭ������������������������Ϊ��ȩ�����Կ�������ɫ�����Ϊ��ɫ��
��ȩ�ܹ�������������ͭ�����������ᣬ������ͭ����ԭΪש��ɫ������ͭ�������������ש��ɫ������
�ʴ�Ϊ����ɫ�����ڣ�ש��ɫ������
��3���������Ҵ������ǻ��ܹ��������Ӧ�����������²�C����Ϊ�Ҵ���Ϊ��ֹ����������������Ӧ��Ӧ�����Ҵ������ų�װ���ڿ���������Ӧ�ȼ���C���ƾ��ƣ�
�ʴ�Ϊ���Ҵ��� C��
��������Ԫ���غ�͵�ʧ���ӣ��������������������������������ϩ������ʵ���������������ɵ�Һ��Ϊ��ȩ��������ȷ��
�ʴ�Ϊ������ȷ��������Ԫ���غ�͵�ʧ���ӣ��������������������������������ϩ������ʵ����������������ȷ��
���� ���⿼�����Ҵ���ԭ��ʵ��̽������ȷ�Ҵ��Ľṹ����Ӧԭ���ǽ���ؼ������ؿ���ѧ��������������������������Ŀ�Ѷ��еȣ�

| A�� | Ԫ��Y����������ϼ�Ϊ+6 | |
| B�� | ���Ӱ뾶�Ĵ�С˳��ΪW��Q��Z��X��Y | |
| C�� | �����£�1molQ���ʺ�������NaOH��Һ��Ӧת��1mol���� | |
| D�� | Ԫ��W������������Ӧ��ˮ�������Ա�Q��ǿ |
| A�� | ����ͱ�ϩ�������2��1 | B�� | �������ϩ�������2��1 | ||
| C�� | C2H6��C2H2�������Ϊ1��1 | D�� | C2H6��C2H2�������2��1 |
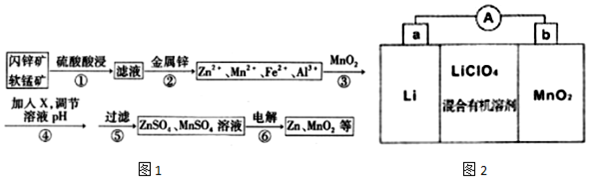
��֪��I����ʯ�����н���Ԫ������Һ�о���������ʽ���ڣ�
���ֽ���������ȫ������pH�����
| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
��1��������з��������Ӧ������MnO2��FeS�����Ṳ��ʱ�е���ɫ������������Һ��Ϊ�ػ�ɫ��д��MnO2��FeS�����Ṳ�ȷ�����Ӧ�Ļ�ѧ����ʽ3MnO2+2FeS+6H2SO4$\frac{\underline{\;\;��\;\;}}{\;}$3MnSO4+Fe2��SO4��3+2S+6H2O��
��2������ڼ������п��Ϊ�˻��ս��������ս�������Ҫ�ɷ���Cu��Cd��
��3���������MnO2����������ԭ��Ӧ�����ӷ���ʽMnO2+2Fe2++4H+=2Fe3++Mn 2++2H2O������X������BD������ĸ��ʾ��
A��Cu2��OH��2CO3 B��MnCO3 C��MgO D��Zn��OH��2
��4�������п���ѭ�����õ�������H2SO4���ѧʽ����
��5��MnO2��Li����LiMnO2���õ�ط�Ӧԭ����ͼ2��ʾ�����е����LiClO4�����ڻ���л��ܼ��У�Li+ͨ�������Ǩ����MnO2�����У�����LiMnO2���ش��������⣺
�����·�еĵ����ƶ���������a������b��������ĸ����
��д��������ӵ�ص������缫��ӦʽMnMnO2+e-+Li+=LiMnO2��
��6����֪��25��ʱ��HCN�ĵ��볣��K=4.9��10-10��H2S�ĵ��볣��K1=1.3��10-7��K2=7.0��10-15����NaCN��Һ��ͨ��������H2S���壬�÷�Ӧ�Ļ�ѧ����ʽΪNaCN+H2S=HCN+NaHS��
| A�� | �������죺2Fe+Al2O3 $\frac{\underline{\;����\;}}{\;}$ 2Al+Fe2O3 | |
| B�� | ��ҵ�̵���N2+3H2 $?_{����}^{���¡���ѹ}$ 2NH3 | |
| C�� | �ô�������ۣ�CO32-+H2O?HCO3-+OH- | |
| D�� | ��ʪ��ĵ���KI��ֽ����Cl2��Cl2+2I-�T2Cl-+I2 |
����MΪ����Ͻ�MHΪ��������ԭ�ӵĴ���Ͻ�KOH��Һ�����Һ�����������أ�����˵������ȷ���ǣ�������
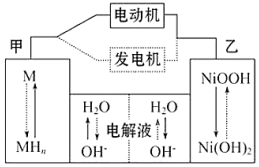
| A�� | ���ʱ����������pH���� | |
| B�� | �綯������ʱ��Һ��OH-����ƶ� | |
| C�� | �ŵ�ʱ������ӦʽΪ��NiOOH+H2O+e-�TNi��OH��2+OH- | |
| D�� | �缫�ܷ�ӦʽΪ��MH+NiOOH$?_{���}^{�ŵ�}$M+Ni��OH��2 |
| A�� | ԭ�Ӱ뾶��С˳��r��Y����r��Z ����r��W����r��M�� | |
| B�� | Z����̬�⻯���W����̬�⻯����ȶ� | |
| C�� | ����ʽΪY5X12������ֻ��3�� | |
| D�� | ������Ԫ��X��Z��W�γɵĻ�������ֻ�й��ۼ��������Ӽ� |
| A�� | ̼��ά���ϳ���ά���ά�������ǽ������� | |
| B�� | ��¯ˮ���е�����ƿ���̼������Һ������ʹ֮ת��Ϊ̼��ƣ��������ȥ | |
| C�� | ʹ�ú�������Ũ�Ƚϴ�ĵ���ˮϴ�·�������ȥ��������ǿ | |
| D�� | ���Ͻ�Ĵ���ʹ�ù鹦��������ʹ�ý�̿���������л���� |