题目内容
13.已知镓(31Ga)和溴(35Br)是第四周期的主族元素.下列分析正确的是( )| A. | 原子半径:Br>Ga>Cl>Al | |
| B. | 碱性:Ga(OH)3>Al(OH)3 酸性:HClO4>HBrO4 | |
| C. | 7935Br与8135Br得电子能力不同 | |
| D. | 与镓同周期且相邻的主族元素,其原子序数为30或32 |
分析 A.同周期自左而右原子半径减小;
B.同主族自上而下金属性增强,金属性越强最高价氧化物对应水化物的碱性越强,同主族自上而下非金属性减弱,非金属性越强最高价氧化物对应水化物的酸性越强;
C.同位素的化学性质相同;
D.镓(31Ga)是第四周期第ⅢA族元素,同周期ⅣA与之相邻.
解答 解:A.同周期自左而右原子半径减小,故原子半径Ga>Br、Al>Cl,故A错误;
B.同主族自上而下金属性增强,故金属性Ga>Al,金属性越强最高价氧化物对应水化物的碱性越强,故碱性Ga(OH)3>Al(OH)3,同主族自上而下非金属性减弱,故非金属性Cl>Br,非金属性越强最高价氧化物对应水化物的酸性越强,则酸性:HClO4>HBrO4,故B正确;
C.7935Br与8135Br互为同位素,同位素的化学性质相同,所以7935Br与8135Br得电子能力相同,故C错误;
D.镓(31Ga)是第四周期第ⅢA族元素,同周期ⅣA与之相邻,原子序数为32,与第ⅡA不相邻,故D错误;
故选B.
点评 本题考查元素周期表结构、元素周期律等,难度不大,注意整体把握元素周期表的结构以及元素周期律,侧重于考查学生对基础知识的综合应用能力.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案
相关题目
3.某同学做了如下实验:下列说法中正确的是( )
| 装置 | 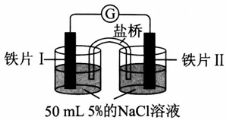 | 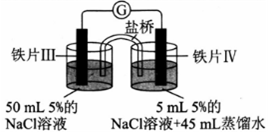 |
| 现象 | 电流计指针未发生偏转 | 电流计指针偏转 |
| A. | 加热铁片I所在烧杯,电流表指针会发生偏转 | |
| B. | 用KSCN溶液检验铁片Ⅲ、IV附近溶液,可判断电池的正、负极 | |
| C. | 铁片I、Ⅲ的腐蚀速率相等 | |
| D. | “电流计指针未发生偏转”,说明铁片I、铁片Ⅱ均未被腐蚀 |
1.化学与生产、生活、社会密切相关.下列说法中正确的是( )
| A. | 过程的自发性只能用于判断过程的方向性,不能确定过程是否一定会发生和过程发生的速率 | |
| B. | 李白诗句“日照香炉生紫烟,遥看瀑布挂前川”,“紫烟”指“香炉”中碘升华的现象 | |
| C. | 用纳米铁粉的吸附性去除污水中的Cu2+、Hg2+等重金属离子 | |
| D. | 用高锰酸钾溶液、酒精、双氧水的氢氧化性进行杀菌消毒 |
8.下列有关实验基本操作的说法正确的是( )
| A. | 用裂化汽油萃取溴水中的溴,将有机层从分液漏斗上口倒出 | |
| B. | 制备氢氧化亚铁时将装有NaOH溶液的胶头滴管插入液面深处并挤压 | |
| C. | 向蔗糖水解后的产物中加入银氨溶液,加热,检验蔗糖是否水解 | |
| D. | 将饱和FeCl3溶液滴入NaOH溶液中制备Fe(OH)3 |
18.下列两组反应,反应类型相同的是( )
| 组别 | Ⅰ | Ⅱ |
| A | 常温下,乙烯和氯气混合 | 乙烷和氯气混合光照 |
| B | 乙酸、乙醇、浓硫酸混合,加热 | 在FeBr3催化下,苯与液溴反应 |
| C | 苯和浓硫酸、浓硝酸混合,加热到50~60℃ | 乙烯在一定条件下与水反应 |
| D | 由乙烯制取聚乙烯 | 蔗糖与稀硫酸混合,加热 |
| A. | A | B. | B | C. | C | D. | D |
5.下列所示的实验,能达到实验目的是( )
| A | B | C | D |
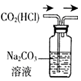 | 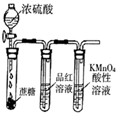 | 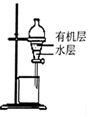 | 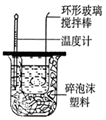 |
| 除去CO2中含有的少量HCl气体 | 说明浓H2SO4具有脱水性,强氧化性,SO2具有漂白性、还原性 | 将有机层从分液漏斗下口放出 | 用于中和反应反应热的测定 |
| A. | A | B. | B | C. | C | D. | D |
1.锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环.下列说法正确的是( )


| A. | 充电时电极b连接电源的正极 | |
| B. | 放电时右侧电解质储罐中的离子总浓度增大 | |
| C. | 放电时电极a连接粗铜可实现粗铜的精炼 | |
| D. | 充电时阴极反应式为2H++2e-=H2↑ |
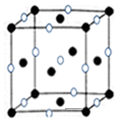 已知A、B、C、D、E、F是周期表前四周期的元素,原子序数依次增大.A的基态原子2p能级有2个单电子;C占整个地壳质量的48.6%,是地壳中含量最多的元素;E的单质常温常压下为黄绿色气体,化学性质十分活泼,具有毒性;F位于ds区,最外能层有单电子,是唯一的能大量天然产出的金属;D与F不同周期,但最外能层电子数相等.
已知A、B、C、D、E、F是周期表前四周期的元素,原子序数依次增大.A的基态原子2p能级有2个单电子;C占整个地壳质量的48.6%,是地壳中含量最多的元素;E的单质常温常压下为黄绿色气体,化学性质十分活泼,具有毒性;F位于ds区,最外能层有单电子,是唯一的能大量天然产出的金属;D与F不同周期,但最外能层电子数相等.