题目内容
 向MgCl2和AlCl3的混合溶液中加入氢氧化钠溶液,所得沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)关系如图所示.则下列说法正确的是( )
向MgCl2和AlCl3的混合溶液中加入氢氧化钠溶液,所得沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)关系如图所示.则下列说法正确的是( )| A、a、c两点沉淀物成份相同,d、e两点沉淀物成份相同 |
| B、在d点,向溶液中加入盐酸,沉淀量将减少 |
| C、b-c段与c-d段溶液中阴离子的物质的量相等 |
| D、在反应过程中,各状态点溶液的pH大小顺序是:e>d>c>a>b |
考点:化学方程式的有关计算,有关混合物反应的计算
专题:计算题
分析:由图象可知,随着氢氧化钠溶液的增加,Mg2+、Al3+逐渐转化为氢氧化物沉淀,发生反应:Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓,b点时沉淀量达到最大,说明此点Mg2+和Al3+完全转化为沉淀,此时溶液中的溶质为NaCl;
继续加入NaOH时,Al(OH)3和NaOH发生反应:Al(OH)3+OH-=AlO2-+2H2O,沉淀逐渐减少,c点溶液中溶质为NaAlO2和NaCl;
d点时,继续滴加NaOH溶液,沉淀的量不再减少,说明此时的沉淀为Mg(OH)2,d点溶液的溶质为NaAlO2和NaCl;e点时,NaOH溶液过量,溶液中的溶质为NaOH、NaAlO2和NaCl,据此分析解答.
继续加入NaOH时,Al(OH)3和NaOH发生反应:Al(OH)3+OH-=AlO2-+2H2O,沉淀逐渐减少,c点溶液中溶质为NaAlO2和NaCl;
d点时,继续滴加NaOH溶液,沉淀的量不再减少,说明此时的沉淀为Mg(OH)2,d点溶液的溶质为NaAlO2和NaCl;e点时,NaOH溶液过量,溶液中的溶质为NaOH、NaAlO2和NaCl,据此分析解答.
解答:
解:由图象可知,随着氢氧化钠溶液的增加,Mg2+、Al3+逐渐转化为氢氧化物沉淀,发生反应:Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓,b点时沉淀量达到最大,说明此点Mg2+和Al3+完全转化为沉淀,此时溶液中的溶质为NaCl;
继续加入NaOH时,Al(OH)3和NaOH发生反应:Al(OH)3+OH-=AlO2-+2H2O,沉淀逐渐减少,c点溶液中溶质为NaAlO2和NaCl;
d点时,继续滴加NaOH溶液,沉淀的量不再减少,说明此时的沉淀为Mg(OH)2,d点溶液的溶质为NaAlO2和NaCl;e点时,NaOH溶液过量,溶液中的溶质为NaOH、NaAlO2和NaCl,
A.通过以上分析知,a点沉淀是Mg(OH)2、Al(OH)3,c点沉淀是Mg(OH)2、Al(OH)3,d、e两点沉淀都是Mg(OH)2,故A正确;
B.在d点,溶质是NaAlO2和NaCl,向溶液中加入少量盐酸,NaAlO2和盐酸反应生成Al(OH)3沉淀,故B错误;
C.b-c段与c-d段溶液中阴离子种类相同,都是AlO2-和Cl-,但b、c、d三点的NaOH的量未知,所以无法判断阴离子物质的量是否相等,故C错误;
D.e点溶液中的溶质是NaOH、NaAlO2和NaCl,d点溶质为NaAlO2和NaCl,c点溶质成分是NaAlO2和NaCl,
d点偏铝酸钠浓度高于c点,b点溶质成分是NaCl,a点溶质成分是MgCl2、AlCl3和NaCl,所以溶液PH大小顺序是e>d>c>b>a,故D错误,
故选A.
继续加入NaOH时,Al(OH)3和NaOH发生反应:Al(OH)3+OH-=AlO2-+2H2O,沉淀逐渐减少,c点溶液中溶质为NaAlO2和NaCl;
d点时,继续滴加NaOH溶液,沉淀的量不再减少,说明此时的沉淀为Mg(OH)2,d点溶液的溶质为NaAlO2和NaCl;e点时,NaOH溶液过量,溶液中的溶质为NaOH、NaAlO2和NaCl,
A.通过以上分析知,a点沉淀是Mg(OH)2、Al(OH)3,c点沉淀是Mg(OH)2、Al(OH)3,d、e两点沉淀都是Mg(OH)2,故A正确;
B.在d点,溶质是NaAlO2和NaCl,向溶液中加入少量盐酸,NaAlO2和盐酸反应生成Al(OH)3沉淀,故B错误;
C.b-c段与c-d段溶液中阴离子种类相同,都是AlO2-和Cl-,但b、c、d三点的NaOH的量未知,所以无法判断阴离子物质的量是否相等,故C错误;
D.e点溶液中的溶质是NaOH、NaAlO2和NaCl,d点溶质为NaAlO2和NaCl,c点溶质成分是NaAlO2和NaCl,
d点偏铝酸钠浓度高于c点,b点溶质成分是NaCl,a点溶质成分是MgCl2、AlCl3和NaCl,所以溶液PH大小顺序是e>d>c>b>a,故D错误,
故选A.
点评:本题考查化学反应图象、镁铝化合物性质等,明确图象中各点的沉淀成分及溶质成分是解本题关键,再结合盐类水解分析解答,难度中等.

练习册系列答案
相关题目
下列说法正确的是( )
| A、纤维素属于髙分子化合物,与淀粉互为同分异构体,水解后均生成葡萄糖 |
| B、2,3一二甲基丁烷的H一NMR上有5个峰 |
| C、含5个碳原子的有机物,每个分子中最多可形成4个C一C单键 |
D、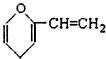 某有机物结构如图所示,该有机物属于芳香族化合物的同分异构体有5种,其中遇FeCl3能显色的有3种 |
体积均为aL的Fe2(SO4)3溶液、ZnSO4溶液、K2SO4溶液,均能与bL1mol?L-1的BaCl2溶液恰好完全反应.则Fe2(SO4)3溶液、ZnSO4溶液、K2SO4溶液的物质的量浓度之比为( )
| A、3:2:2 |
| B、1:2:3 |
| C、1:3:3 |
| D、3:1:1 |
将24ml的NO2、NO混合气体和12ml的O2通入倒立在水槽中盛有水的量筒内,充分反应后,量筒里液面上升,最终剩余3ml气体,则原混合气体中NO的体积为( )
①16ml ②16.5ml ③7.5ml ④6ml ⑤18ml ⑥12ml.
①16ml ②16.5ml ③7.5ml ④6ml ⑤18ml ⑥12ml.
| A、①② | B、⑤⑥ | C、③④ | D、②④ |
在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:SnCl2+Cl-+H3AsO3+H+-As+SnCl
+M(未配平),关于该反应的说法中正确的组合是( )
①氧化剂是H3AsO3
②还原性:Cl->As
③每生成0.1mol的As,还原剂失去的电子为0.3mol
④M为OH-
⑤SnCl
是氧化产物
⑥H+前面的配平系数为6.
2- 0 |
①氧化剂是H3AsO3
②还原性:Cl->As
③每生成0.1mol的As,还原剂失去的电子为0.3mol
④M为OH-
⑤SnCl
2- 0 |
⑥H+前面的配平系数为6.
| A、①③⑤⑥ | B、①②④⑤ |
| C、①②③④ | D、只有①③⑥ |
下列各组分子中,都属于含极性键的非极性分子的是( )
| A、CO2 H2S |
| B、C2H4 CH4 |
| C、C60 C2H4 |
| D、NH3 HCl |
在其它条件不变时,10℃时以某物质表示的反应速率为3mol/(L?s),已知温度每升高10℃反应速率是原来的2倍,则温度为50℃时,该反应的速率为( )
| A、48 mol/(L?s) |
| B、36mol/(L?s) |
| C、24 mol/(L?s) |
| D、12 mol/(L?s) |