��Ŀ����
|
ij�¶�ʱ����һ���Ϊ2 L���ܱ������У�ͨ��112 g N2��24 g��H2����ʱ������ѹǿΪp MPa���ڸ��¶Ⱥʹ��������£�H2��N2��Ӧ���ﵽƽ�⣬���ƽ��ʱѹǿΪ0.95p MPa������˵������ȷ���� | |
| [����] | |
A�� |
ƽ��ʱ��N2���ʵ�����3.6 mol |
B�� |
ƽ��ʱ��H2�����ʵ�����10.8 mol |
C�� |
ƽ��ʱ��N2��ת����Ϊ10�� |
D�� |
NH3�����������10�� |
�𰸣�D
������
������
|
������ͬ��ͬ��������£��������ʵ���֮�ȵ���ѹǿ�ȣ� �������ƽ��ʱ��x mol��N2ת��ΪNH3�����У� ������������������������N2������3H2 ������ʼ���ʵ���/mol����4��������12��������������0 ����ƽ�����ʵ���/mol����4��x����12��3x����������2x �������� ������ƽ��ʱ��n(N2)��4 mol��0.4 mol��3.6 mol��A��ȷ ��������������n(H2)��12 mol��1.2 mol��10.8 mol��B��ȷ ����ƽ��ʱN2��ת���ʣ� ������������w(N2)�� ����ƽ��ʱNH3��������� ����w(NH3)�� |

��ϰ��ϵ�д�
 Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д�
Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д�
�����Ŀ
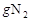 ��24
��24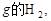 ��ʱ������ѹǿΪp����ѹ���ڸ��¶Ⱥʹ��������£�H2��N2��Ӧ�ﵽƽ�⣬���ƽ��ʱѹǿΪ0.95p����ѹ������˵������ȷ���ǣ�
��
��ʱ������ѹǿΪp����ѹ���ڸ��¶Ⱥʹ��������£�H2��N2��Ӧ�ﵽƽ�⣬���ƽ��ʱѹǿΪ0.95p����ѹ������˵������ȷ���ǣ�
��