题目内容
5.下列有关概念说法正确的是( )| A. | D2、T2、H2互为同素异形体 | B. | 石墨、金刚石互为同位素 | ||
| C. | 甲烷和异丁烷互为同系物 | D. | 乙烷和乙烯互为同分异构体 |
分析 A.同素异形体是同种元素形成的不同单质,同素异形体首先是单质,其次是同种元素;
B.质子数相同中子数不同的原子互称同位素;
C.结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;
D.具有相同分子式而结构不同的化合物互为同分异构体;
解答 解:A.D2、T2、H2是同一物质,都是氢气,不符合同素异形体概念,仅仅是D2、T2、H2组成中氢原子中中子数不同,故A错误;
B.石墨、金刚石是由碳元素组成的不同单质,属于同素异形体,故B错误;
C.甲烷和异丁烷结构简式分别为CH4和CH3(CH2)2CH3结构相似,分子组成相差三个CH2原子团,互为同系物,故C正确;
D.乙烷属于饱和烃分子式为C2H6,乙烯分子中含有碳碳双键分子式为C2H4,它们分子式不同,不符合同分异构体的要求,故D错误;
故选C.
点评 本题考查化学“四同”,题目难度不大,注意把握概念的理解和“四同”间的异同是解决此类题的关键之所在.

练习册系列答案
相关题目
16.将含有O2和CH4的混合气体置于盛有23.4g Na2O2的密闭容器中,电火花点燃,反应结束,容器内的压强为零(温度150℃),将残留物溶于水,无气体产生,下列叙述正确的是( )
| A. | 原混合气体中O2和CH4的体积比为2:1 | |
| B. | 残留物中只有Na2CO3 | |
| C. | 原混合气体中O2和CH4的物质的量之比为1:2 | |
| D. | 残留物只有Na2CO3和NaOH |
20.下列说法中正确的组合是( )
①质子数相同的微粒一定是同种元素
②电子数相同的微粒不一定是同一种元素
③化学键是两个原子之间的相互作用力
④离子键和极性键只存在于化合物中
⑤化学键的断裂和形成是化学反应能量变化的主要原因.
①质子数相同的微粒一定是同种元素
②电子数相同的微粒不一定是同一种元素
③化学键是两个原子之间的相互作用力
④离子键和极性键只存在于化合物中
⑤化学键的断裂和形成是化学反应能量变化的主要原因.
| A. | ①②③ | B. | ①③④ | C. | ②④⑤ | D. | ②③⑤ |
10.下列化学用语正确的是( )
| A. | H2O2的电子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-H+ | |
| B. | 次氯酸的结构式:H-O-Cl | |
| C. | S2-的结构示意图: | |
| D. | CO2的比例模型: |
14.二氧化硫能使溴水褪色,说明二氧化硫具有( )
| A. | 氧化性 | B. | 还原性 | C. | 漂白性 | D. | 酸性 |
15.下列各组元素性质或原子结构的递变,叙述不正确的是( )
| A. | Na、Mg、Al原子最外层电子数依次增多 | |
| B. | P、S、Cl元素最高正化合价依次增大 | |
| C. | N、O、F得电子能力依次减弱 | |
| D. | LiOH、NaOH、KOH的碱性逐渐增强 |
 试回答下列问题:
试回答下列问题: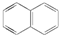 .萘的一氯代物有2种可能的结构,萘的六氯代物有10种可能的结构.
.萘的一氯代物有2种可能的结构,萘的六氯代物有10种可能的结构.