题目内容
乳酸是一种体内代谢物,其结构简式为 试回答:
试回答:
(1)乳酸分子中含有的官能团是 和 .(填名称)
(2)乳酸不能发生的反应是 (填序号)
A.酯化反应 B.取代反应 C.加成反应 D.消去反应.
 试回答:
试回答:(1)乳酸分子中含有的官能团是
(2)乳酸不能发生的反应是
A.酯化反应 B.取代反应 C.加成反应 D.消去反应.
考点:有机物的结构和性质
专题:
分析:由乳酸结构简式可知,分子中含-OH、-COOH,结合醇、羧酸的性质来解答.
解答:
解:(1)乳酸结构简式可知,分子中含-OH、-COOH,名称分别为羟基、羧基,故答案为:羟基;羧基;
(2)含-OH可发生酯化反应、取代反应、消去反应,含-COOH可发生酯化反应、取代反应,不能发生加成反应,故答案为:C.
(2)含-OH可发生酯化反应、取代反应、消去反应,含-COOH可发生酯化反应、取代反应,不能发生加成反应,故答案为:C.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重醇、羧酸性质的考查,题目难度不大.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
关于物质的分类正确的是( )
| A、SO2、CO2、CO、NO2都是酸性氧化物 |
| B、Na2O、Na2O2、Fe2O3、CuO都是碱性氧化物 |
| C、HCl、HClO、HNO3、HClO4都是强酸 |
| D、NaOH、KOH、Ba(OH)2、Ca(OH)2都是强碱 |
下列实验操作正确的是( )
| A、用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 |
| B、蒸馏石油时,应使温度计水银球放在蒸馏烧瓶的支管口处 |
| C、分液操作时,上层液体经分液漏斗下口放出 |
| D、为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行 |
制备晶体硅的热方程式为 SiHCl3(l)+H2(g)=Si(s)+3HCl(g)△H=+238KJ/mol,
已知SiHCl3(l)=SiHCl3(g)△H=+10KJ/mol,相关键能数据如下表:则晶体硅的键能为( )
已知SiHCl3(l)=SiHCl3(g)△H=+10KJ/mol,相关键能数据如下表:则晶体硅的键能为( )
| SiHCl3(g) Si-H | SiHCl3(g) Si-Cl | H2(g) H-H | HCl(g) H-Cl | |
| 键能(KJ/mol) | 377 | 360 | 436 | 431 |
| A、186KJ/mol |
| B、181KJ/mol |
| C、372KJ/mol |
| D、362KJ/mol |
下列实验操作中错误的是( )
| A、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、蒸发结晶时应将溶液蒸干 |
| D、称量NaOH,称量物放在小烧杯中置于托盘天平的左盘,砝码放在托盘天平的右盘中 |
下列实验操作中不会使用到玻璃棒的是( )
| A、分离食盐水中的泥沙 |
| B、浓硫酸的稀释 |
| C、测定某溶液的pH值 |
| D、蒸馏法分离酒精和水 |
室温时,盐酸和硫酸的混合溶液20ml,向混合溶液中逐滴加入0.05mol?L-1Ba(OH)2溶液时,生成的BaSO4和pH的变化如图所示(不考虑溶液混合时体积的变化).下列说法正确的是( )
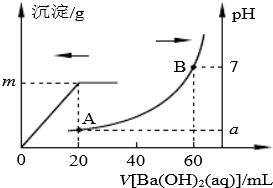

| A、图中A点对应溶液的pH=l |
| B、生成沉淀的最大质量m=2.33 g |
| C、原混合溶液中盐酸物质的量浓度为0.1 mol?L-1 |
| D、当V[Ba(OH)2(aq)]=10 mL时,发生反应的离子方程式为:Ba2++SO42-═BaSO4↓ |
对于可逆反应A(g)+3B(g)?2C(g),在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
| A、V(A)=0.5 mol/(L?min) |
| B、V(B)=1.2 mol/(L?min) |
| C、V(C)=0.4 mol/(L?min ) |
| D、V(C)=1.1 mol/(L?min) |
 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此回答下列问题:
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此回答下列问题: