题目内容
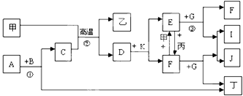 下列各物质是中学化学中常见的物质,甲为常见金属单质,乙、丙、丁是非金属单质,其它为化合物,B、D分别为黑色粉末和黑色晶体,G为淡黄色固体,J为生活中常见的调味品,I为红褐色固体,①是实验室制取丁的反应之一,F为棕黄色溶液.各物质间的转化如如图所示,回答下列各问题(部分生成物未列出):
下列各物质是中学化学中常见的物质,甲为常见金属单质,乙、丙、丁是非金属单质,其它为化合物,B、D分别为黑色粉末和黑色晶体,G为淡黄色固体,J为生活中常见的调味品,I为红褐色固体,①是实验室制取丁的反应之一,F为棕黄色溶液.各物质间的转化如如图所示,回答下列各问题(部分生成物未列出):(1)写出乙的化学式
(2)写出G的一种用途
(3)写出B与K反应的化学方程式:
(4)整个转换过程中属于氧化还原反应的有
(5)写出反应③E与G按物质的量之比2:1的反应的离子方程式
考点:无机物的推断
专题:推断题
分析:D为黑色晶体,应为Fe3O4,J为生活中常见的调味品,应为NaCl,I为红褐色固体,应为Fe(OH)3,甲为常见金属单质,乙、丙、丁是气体单质,可知甲和C的反应应为Fe和水蒸气在高温下的反应,则甲为Fe,C为H2O,乙为H2,由E和F的相互转化可知K应为HCl,E为FeCl2,F为FeCl3,则丙为Cl2,G为淡黄色固体,应为Na2O2,则丁为O2,A为H2O2,B为MnO2,结合对应物质的性质以及题目要求解答该题.
解答:
解:D为黑色晶体,应为Fe3O4,J为生活中常见的调味品,应为NaCl,I为红褐色固体,应为Fe(OH)3,甲为常见金属单质,乙、丙、丁是气体单质,可知甲和C的反应应为Fe和水蒸气在高温下的反应,则甲为Fe,C为H2O,乙为H2,由E和F的相互转化可知K应为HCl,E为FeCl2,F为FeCl3,则丙为Cl2,G为淡黄色固体,应为Na2O2,则丁为O2,A为H2O2,B为MnO2,
(1)由以上分析可知乙为H2,A为H2O2,电子式为 ,甲为Fe,位于周期表第四周期第Ⅷ族,
,甲为Fe,位于周期表第四周期第Ⅷ族,
故答案为:H2; ;第四周期第Ⅷ族;
;第四周期第Ⅷ族;
(2)G为Na2O2,可用作供氧剂,故答案为:供氧剂;
(3)B与K的反应常用于实验室制备氯气,方程式为MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
(4)题中所有反应都涉及氧化还原反应,共6个,故答案为:6;
(5)反应③FeCl2与Na2O2按物质的量之比2:1的反应,二者恰好发生氧化还原反应,反应的离子方程式为6Fe2++3Na2O2+6H2O=4Fe(OH)3+2Fe3++6Na+,
故答案为:6Fe2++3Na2O2+6H2O=4Fe(OH)3+2Fe3++6Na+.
(1)由以上分析可知乙为H2,A为H2O2,电子式为
 ,甲为Fe,位于周期表第四周期第Ⅷ族,
,甲为Fe,位于周期表第四周期第Ⅷ族,故答案为:H2;
 ;第四周期第Ⅷ族;
;第四周期第Ⅷ族;(2)G为Na2O2,可用作供氧剂,故答案为:供氧剂;
(3)B与K的反应常用于实验室制备氯气,方程式为MnO2+4HCl(浓)
| ||
| ||
(4)题中所有反应都涉及氧化还原反应,共6个,故答案为:6;
(5)反应③FeCl2与Na2O2按物质的量之比2:1的反应,二者恰好发生氧化还原反应,反应的离子方程式为6Fe2++3Na2O2+6H2O=4Fe(OH)3+2Fe3++6Na+,
故答案为:6Fe2++3Na2O2+6H2O=4Fe(OH)3+2Fe3++6Na+.
点评:本题考查无机物的推断,题目难度不大,本题注意根据物质的性质、特征作为突破口进行推断,学习中注意牢固把握元素化合物的性质,不要忽视物质的用途.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
原子序数为26的Fe核外未成对的电子数为( )
| A、5 | B、4 | C、3 | D、2 |
下列各物质中,所有原子都满足最外层8电子结构的是( )
| A、BeCl2 |
| B、PCl3 |
| C、NH3 |
| D、PCl5 |
已知某元素的前8个电离能(I1/kJ?mol-1):I1=577,I2=1820,I3=2740,I4=11600,I5=14800,I6=18400,I7=23400,I8=27500.该元素原子的最外层有几个电子?( )
| A、1个 | B、2个 | C、3个 | D、4个 |
下列说法正确的是( )
| A、可用碘水鉴别苯、四氯化碳、乙醇三种无色液体 |
| B、取0.2mol NaCl固体于烧杯中,加入200 mL蒸馏水充分搅拌可配成1mol/L的NaCl溶液 |
| C、测定溶液的酸碱性时,应先将pH试纸润湿,然后进行检测 |
| D、为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量应相等 |
下列实验方案可行的是( )
| A、在淀粉溶液中加稀硫酸充分反应后,再加入银氨溶液,可检验淀粉的水解产物 |
| B、用溴水可以鉴别苯、乙醇、四氯化碳三种液体 |
| C、除去苯中的苯酚,可加入NaOH溶液后再分液 |
| D、将氯乙烷与NaOH的乙醇溶液共热,将产生的气体直接通入酸性高锰酸钾溶液中,溶液褪色,证明氯乙烷发生了消去反应. |
下列能大量共存且溶液为无色透明的离子组是( )
| A、Al3+、Na+、HCO3-、Cl- |
| B、Fe3+、NO3-、Cl-、SO42- |
| C、Na+、H+、SO32-、NO3- |
| D、SiO32-、Na+、K+、CO32- |
下列除去杂质的方法正确的是( )
| A、除去 CO2 中混有的 CO:用澄清石灰水洗气 |
| B、除去 BaCO3 固体中混有的 BaSO4:加过量盐酸后,过滤、洗涤 |
| C、除去 FeCl2 溶液中混有的 FeCl3:加入过量铁粉,过滤 |
| D、除去 Cu 粉中混有的 CuO:加适量稀硝酸后,过滤、洗涤 |