题目内容
表中根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 某溶液W进行焰色反应实验 | 焰色为黄色 | W一定是钠盐溶液 |
| B | 蘸有浓氨水的玻璃棒靠近溶液X | 有白烟产生 | X可能是浓盐酸 |
| C | 强酸性溶液Y中加入Ba(NO3)2溶液,静置后再加入KSCN溶液 | 先有白色沉淀,后溶液又变红 | Y中一定含有SO42-和Fe3+ |
| D | 气态炔烃Z通入pH=α的溴水中 | 溴水褪色,溶液的pH>α | Z与溴发生了取代反应 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.焰色反应为元素的性质;
B.浓硝酸、浓盐酸均易挥发;
C.白色沉淀为硫酸钡,溶液变红说明存在Fe3+,但硝酸盐在酸性溶液中具有强氧化性;
D.pH变大,应为发生加成反应.
B.浓硝酸、浓盐酸均易挥发;
C.白色沉淀为硫酸钡,溶液变红说明存在Fe3+,但硝酸盐在酸性溶液中具有强氧化性;
D.pH变大,应为发生加成反应.
解答:
解:A.焰色反应为元素的性质,则焰色为黄色,可知W可能是钠盐溶液或NaOH等,故A错误;
B.浓硝酸、浓盐酸均易挥发,生成白烟为铵盐,则X可能是浓盐酸,故B正确;
C.白色沉淀为硫酸钡,溶液变红说明存在Fe3+,但硝酸盐在酸性溶液中具有强氧化性,则Y中可能含有SO42-和Fe3+,或Fe2+,故C错误;
D.pH变大,应为发生加成反应,若发生取代反应,pH变小,故D错误;
故选B.
B.浓硝酸、浓盐酸均易挥发,生成白烟为铵盐,则X可能是浓盐酸,故B正确;
C.白色沉淀为硫酸钡,溶液变红说明存在Fe3+,但硝酸盐在酸性溶液中具有强氧化性,则Y中可能含有SO42-和Fe3+,或Fe2+,故C错误;
D.pH变大,应为发生加成反应,若发生取代反应,pH变小,故D错误;
故选B.
点评:本题考查化学实验方案的评价,为高频考点,涉及焰色反应、离子检验、氧化还原反应及物质的性质等,把握物质的性质、化学反应原理为解答的关键,侧重性质与原理的考查,注意实验的可行性、评价性分析,选项C为解答的难点,题目难度不大.

练习册系列答案
相关题目
利用下列实验装置进行的相应实验,不能达到实验目的是( )
A、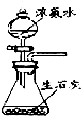 可制取氨气 |
B、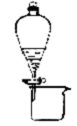 可分离CH3CH2OH和CH3COOC2H5混合液 |
C、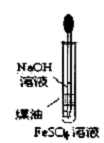 可制备Fe(OH)2并容易观察到白色沉淀 |
D、 可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂自性、还原性 |
关于下列各实验装置的叙述中,不正确的是( )
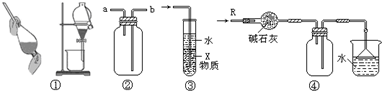

| A、装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 |
| B、装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 |
| C、装置①可用于分离乙醇和水的混合物 |
| D、装置④可用于干燥、收集氨气,并吸收多余的氨气 |
饱和氯水中存在如下平衡:①Cl2+H2O═H++Cl-+HClO;②HClO═H++ClO-,将饱和氯水倒入试管中分别进行下列实验,相应分析结论错误的是( )
| A、加入CaCO3悬浊液,CaCO3的溶解平衡向右移动 |
| B、加入澄清石灰水,c(H+)一定减小 |
| C、加入一定量NaOH溶液后,溶液中离子浓度的关系可能为c(Cl-)+c(ClO-)=c(Na+) |
| D、通入过量Cl2,①、②均向右移动,溶液pH减小 |
化学与生产、生活密切相关.下列叙述错误的是( )
| A、光导纤维遇强碱会“断路” |
| B、从海带中提取碘的过程涉及氧化还原反应 |
| C、钠可把钛、锆、铌、钽等金属从其熔融卤化物里还原出来 |
| D、绿色化学的核心是应用化学原理对环境污染进行治理 |
 过二硫酸的化学式为H2S2O8,硫元素的形式氧化态可看作是+7,所以是一种强氧化剂.工业上常用电解硫酸和硫酸钾的混合溶液制过二硫酸钾,且在65℃时熔化并分解.电解反应的离子方程式是:2HSO
过二硫酸的化学式为H2S2O8,硫元素的形式氧化态可看作是+7,所以是一种强氧化剂.工业上常用电解硫酸和硫酸钾的混合溶液制过二硫酸钾,且在65℃时熔化并分解.电解反应的离子方程式是:2HSO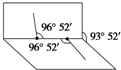 已知H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角为93°52′,而两个O-H键与O-O键的夹角均为96°52′.
已知H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角为93°52′,而两个O-H键与O-O键的夹角均为96°52′.