题目内容
标准状况下,甲烷和一氧化碳的混合气体共8.96L,其质量为7.6g,则混合气体中甲烷的体积为 ,一氧化碳的质量为 .
考点:有关混合物反应的计算
专题:
分析:由平均摩尔质量=
来计算,由质量和物质的量的关系列方程解出甲烷的物质的量,再计算混合气体中甲烷的体积和一氧化碳的质量.
| m |
| n |
解答:
解:(1)标准状况下,8.96L气体的物质的量为:n=
=0.4mol,设甲烷的物质的量为x,CO的物质的量为y,
则:x+y=0.4mol、16x+28y=7.6g,
解得:x=0.3mol、y=0.1mol,
混合气体中甲烷的体积为:0.3mol×22.4mol/L=6.72L;
一氧化碳的质量为:0.1mol×28g/mol=2.8g,
故答案为:6.72L;2.8g.
| 8.96L |
| 22.4L/mol |
则:x+y=0.4mol、16x+28y=7.6g,
解得:x=0.3mol、y=0.1mol,
混合气体中甲烷的体积为:0.3mol×22.4mol/L=6.72L;
一氧化碳的质量为:0.1mol×28g/mol=2.8g,
故答案为:6.72L;2.8g.
点评:本题考查了混合物的化学计算,题目难度不大,试题侧重基础知识的考查,明确物质的量与气体摩尔体积、摩尔质量之间的转化关系为解答关键,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
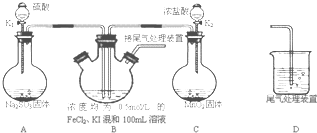
某课外实验小组设计的下列实验合理的是( )
A、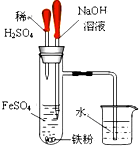 制备并观察氢氧化亚铁 |
B、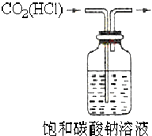 除去二氧化碳中的氯化氢 |
C、 制取干燥、纯净氯气 |
D、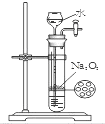 制取少量氧气 |
下列离子方程式书写正确的是( )
| A、氯气通入碘化钾溶液:Cl2+I-=Cl-+I2 |
| B、稀盐酸与氨水混合:H++OH-=H2O |
| C、碳酸钠溶液与稀盐酸混合:CO32-+2H+=H2O+CO2↑ |
| D、稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
2011年为国际化学年,主题为“化学--我们的生活,我们的未来”.下列说法正确的是( )
| A、制作航天服的聚酯纤维和用于光缆通信的晶体硅都是新型无机非金属材料 |
| B、金刚砂的成分是Al2O3,可用作砂纸、砂轮的磨料 |
| C、石油化工广泛使用过渡元素做催化剂并加入少量稀土元素改善催化剂的性能 |
| D、福尔马林(甲醛溶液)可用于浸泡生肉及海产品以防腐保鲜 |

 -R+HX
-R+HX -R
-R -COOH
-COOH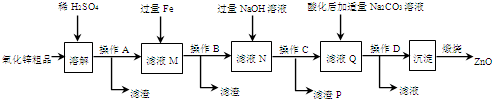
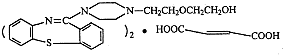 ,它的合成路线如下:
,它的合成路线如下: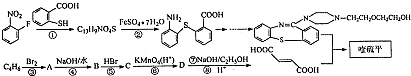
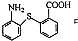 中除硫醚键(一S一)外,还含有的官能团名称为
中除硫醚键(一S一)外,还含有的官能团名称为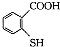 在一定条件下发生缩聚反应的化学方程式为
在一定条件下发生缩聚反应的化学方程式为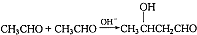 请设计合理方案,用乙醇制取上述流程中的C4H6(其他无机原料自选,用反应流程图表示,并注明必要的反应条件).
请设计合理方案,用乙醇制取上述流程中的C4H6(其他无机原料自选,用反应流程图表示,并注明必要的反应条件).