题目内容
16.Na2SO3是一种重要的化下原料,但较易变质.(1)某小组同学欲在实验室测定某Na2SO3样品的纯度,利用如图装置进行实验.
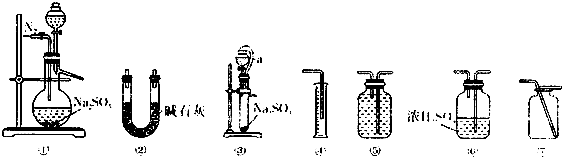
方案一:选择装置①和②进行实验时,为使结果更精确还应选择装置⑥,装置①的分液漏斗中添加浓硫酸(填物质名称)较理想;装置①中反应前后通入N2的目的是反应前排净装置中的空气,反应后将装置中的SO2全部吹出.
方案二:选择装置③和④进行实验时,还应选择装置⑤,此装置中应盛装饱和亚硫酸氢钠溶液(填物质名称),装置③中a 管的作用是平衡压强使分液漏斗中的液体顺利滴下,并使测量结果更精确.
(2)将20.0g Na2SO3固体溶于120mL水配成溶液,再将足量硫粉用少许乙醇和水浸润,加入上述溶液,混合加热可制得Na2SO3.
①硫粉用少许乙醇和水浸润的目的是BD(填字母).
A.增加反应体系的pH C.降低反应的活化能
B.增大反应物接触而积 D.加快反应速率
②设Na2SO3完全反应,将上述反应液经过滤、蒸发、浓缩后,冷却至70℃时,溶液恰好达到饱和,请列式计算此时溶液的体积约为$\frac{20.0g×\frac{158g/mol}{126g/mol}×\frac{212g+100g}{212g}}{1.17g/c{m}^{3}}$=31.5cm3.(结果精确到0.1)(已知:70℃时,Na2S2O3的溶解度为212g,饱和溶液的密度为1.17g/cm3).
分析 (1)方案一:测定某Na2SO3样品的纯度,利用装置①②原理是样品和浓硫酸反应生成二氧化硫气体通过浓硫酸干燥后进入装置②被碱石灰吸收测定增重为二氧化硫质量,结合硫元素守恒计算纯度,为防止装置内空气中的二氧化碳、水蒸气干扰测定,需要开始通过氮气排净装置内空气,反应结束通氮气吧生成的二氧化硫全部排入碱石灰吸收;
反案二:选择装置③和④进行实验时,是利用排液体量气方法测定生成气体的体积,需要装置⑤,所盛溶液不能和二氧化硫发生反应,应选择饱和亚硫酸氢钠溶液,装置③中a 管的作用平衡压强使漏斗中液体顺利流下;
(2)①依据影响化学反应速率的因素分析判断选项;
②计算亚硫酸钠物质的量得到硫代硫酸钠物质的量,计算得到溶质质量,形成的饱和溶液溶质质量分数=$\frac{S}{100+S}$×100%,据此计算溶液质量,溶液体积V=$\frac{m}{ρ}$;
解答 解:(1)方案一:测定某Na2SO3样品的纯度,利用装置①②原理是样品和浓硫酸反应生成二氧化硫气体通过浓硫酸干燥后进入装置②被碱石灰吸收测定增重为二氧化硫质量,干燥装置选择③,导气管长进短出,结合硫元素守恒计算纯度,为防止装置内空气中的二氧化碳、水蒸气干扰测定,需要开始通过氮气排净装置内空气,反应结束通氮气吧生成的二氧化硫全部排入碱石灰吸收,;
故答案为:⑥;浓硫酸;反应前排净装置中的空气,反应后将装置中的SO2全部吹出;
方案二:选择装置③和④进行实验时,是利用排液体量气方法测定生成气体的体积,需要装置⑤,所盛溶液不能和二氧化硫发生反应,应选择饱和亚硫酸氢钠溶液,导气管短进长出,装置③中a 管的作用平衡压强使漏斗中液体顺利流下,
故答案为:⑤;饱和亚硫酸氢钠溶液;平衡压强使分液漏斗中的液体顺利滴下,并使测量结果更精确;
(2)①依据影响化学反应速率的因素分析判断选项,硫粉用少许乙醇和水浸润的目的是增大接触面积,加快反应速率,故选BD,
故答案为:BD;
②计算亚硫酸钠物质的量得到硫代硫酸钠物质的量=$\frac{20g}{126g/mol}$,硫元素守恒计算得到溶质硫代硫酸钠质量=$\frac{20g}{126g/mol}$×158g/mol,形成的饱和溶液溶质质量分数=$\frac{S}{100+S}$×100%=$\frac{212g}{100g+212g}$×100%,据此计算溶液质量=$\frac{\frac{20g}{126g/mol}×158g/mol}{\frac{212g}{212g+100g}×100%}$,溶液体积V=$\frac{m}{ρ}$=$\frac{20.0g×\frac{158g/mol}{126g/mol}×\frac{212g+100g}{212g}}{1.17g/c{m}^{3}}$=31.5cm3,
故答案为:$\frac{20.0g×\frac{158g/mol}{126g/mol}×\frac{212g+100g}{212g}}{1.17g/c{m}^{3}}$×100%=31.5cm3;
点评 本题考查了物质组成和成分纯度的实验过程分析和计算应用,主要是装置作用、试剂选择和装置连接,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 ;元素⑩名称为Br.
;元素⑩名称为Br.(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的电子式是:
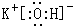 .
.(3)元素⑤与⑦形成化合物的化学式为AlCl3;实验测得,当此化合物在液态或固态时不导电,溶解于水时能导电,由此判断该化合物属于共价化合物.
(4)元素③、⑥、⑦形成的气态氢化物中,沸点最高的物质的化学式是H2O,原因是H2O分子间含有氢键.
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是S2->Cl->O2-.
| A. | .苯及其同系物没有官能团 | B. | 卤代烃中至少含有3种元素 | ||
| C. | .醛的官能团为CHO- | D. | 羧酸和酯的官能团相同 |
(1)Fe单质为体心立方晶体,晶胞中铁原子的配位数为8,基态铁原子有4个未成对电子,Fe3+的电子排布式为1s22s22p63s23p63d6;.
(2)硝酸钾中NO3-的空间构型为平面正三角形,写出与NO3-互为等电子体的一种非极性分子化学式BF3[SO3(g)、BBr3等].
(3)6氨基青霉烷酸的结构如图1所示,其中采用sp3杂化的原子有C、N、O、S.
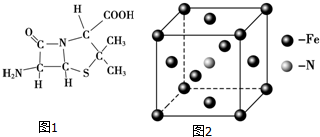
(4)下列说法正确的有a(填字母序号).
a.乙醇分子间可形成氢键,导致其沸点比氯乙烷高
b.钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显-1价
c.聚乙烯(
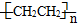 )分子中有5n个σ键
)分子中有5n个σ键d.由下表中数据可确定在反应Si(s)+O2(g)═SiO2(s)中,每生成60g SiO2放出的能量为(2c-a-b) kJ
| 化学键 | Si-Si | O═O | Si-O |
| 键能(kJ•mol-1) | a | b | c |
| A. | 将少量Cl2通入FeBr2溶液中:Cl2+2Br-═Br2+2Cl- | |
| B. | 将足量Cl2通入FeBr2溶液中:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| C. | 将少量Cl2通入FeI2溶液中:2Fe2++2I-+3Cl2═2Fe3++2I2+6Cl- | |
| D. | 将672mLCl2(标况)通入250mL 0.1molL-1的FeI2溶液中:2Fe2++10I-+6Cl2═12Cl-+5I2+2Fe3+ |
| A. | 断开一个N≡N,同时有六个N-H键生成 | |
| B. | 生成氨的速率与分解氨的速率相等 | |
| C. | N2、H2,、NH3的质量分数不再变化 | |
| D. | 混合气体总压不再改变 |
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:
(1)以上步骤有错误的是(填编号)①,该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”)偏大.
(2)判断滴定终点的现象是:无色变为粉红色,半分钟内不变色.
(3)根据下列数据:请计算待测盐酸溶液的浓度:0.20mol/L.
滴定次数 | 待测体积(mL) | 标准烧碱体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 2.00 | 24.10 |
| 第三次 | 20.00 | 4.00- | 24.00 |
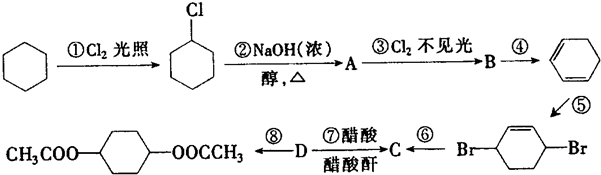
 ,C
,C .
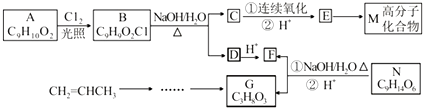
.
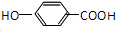 .
. .
.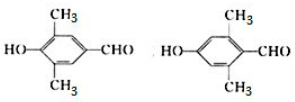 .
. .
.