题目内容
11.某同学称取一定质量的AlCl3固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶液中逐滴加入NaOH溶液如图甲所示.滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示.
请回答下列问题:
(1)溶解AlCl3固体所用的玻璃仪器有bd(填字母).
a.天平 b.烧杯 c.漏斗 d.玻璃棒
(2)OA段反应的离子方程式为OH-+H+═H2O.
(3)BC段反应的离子方程式为OH-+Al(OH)3=AlO2-+2H2O.
(4)在B点对应的溶液中滴加AgNO3溶液,观察到的现象是立即出现白色沉淀,涉及到得离子方程式为Ag++Cl-=AgCl↓.
分析 首先发生NaOH+HCl═NaCl+H2O,盐酸反应完毕,再发生反应3NaOH+AlCl3=3NaCl+Al(OH)3↓,最后发生NaOH+Al(OH)3=NaAlO2+2H2O,沉淀溶解,
(1)溶解AlCl3固体,应该在烧杯里并且用玻璃棒不断的搅拌加速溶解;
(2)根据以上分析OA段反应为酸碱中和反应;
(3)BC段反应是氢氧化铝溶于碱溶液生成偏铝酸钠和水;
(4)据以上分析B点时氢氧化铝刚好完全沉淀,溶液的只剩NaCl,所以滴加AgNO3溶液,观察到的现象立即出现白色沉淀.
解答 解:首先发生NaOH+HCl═NaCl+H2O,盐酸反应完毕,再发生反应3NaOH+AlCl3=3NaCl+Al(OH)3↓,最后发生NaOH+Al(OH)3=NaAlO2+2H2O,沉淀溶解,
(1)溶解AlCl3固体,应该在烧杯里并且用玻璃棒不断的搅拌,故选:bd,
故答案为:bd;
(2)根据以上分析OA段反应的离子方程式为OH-+H+═H2O,
故答案为:OH-+H+═H2O;
(3)根据以上分析BC段反应的离子方程式为OH-+Al(OH)3=AlO2-+2H2O,
故答案为:OH-+Al(OH)3=AlO2-+2H2O;
(4)根据以上分析B点时氢氧化铝刚好完全沉淀,溶液的只剩NaCl,所以滴加AgNO3溶液,观察到的现象立即出现白色沉淀,反应的离子方程式为:Ag++Cl-=AgCl↓,
故答案:立即出现白色沉淀;Ag++Cl-=AgCl↓.
点评 本题以图象形式考查混合物的有关计算、物质性质分析,清楚各阶段发生的反应是关键,题目难度中等.

练习册系列答案
相关题目
20.下列有关氧元素及其化合物表示正确的是( )
| A. | 质子数为8、中子数为10的氧原子:${\;}_{16}^{8}$O | |
| B. | 过氧化氢的电子式: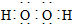 | |
| C. | 氧原子的价电子排布图: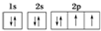 | |
| D. | 次氯酸的结构式:H-Cl-O |
1.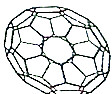 目前,化学家们已经找到十余种富勒烯家族的Cn,它们分子结构中都由正五边形和正六边形构成的封闭的凸多面体,C60就是其中的一种富勒烯,其结构如图所示,下列物质不属于富勒烯家族的是( )
目前,化学家们已经找到十余种富勒烯家族的Cn,它们分子结构中都由正五边形和正六边形构成的封闭的凸多面体,C60就是其中的一种富勒烯,其结构如图所示,下列物质不属于富勒烯家族的是( )
 目前,化学家们已经找到十余种富勒烯家族的Cn,它们分子结构中都由正五边形和正六边形构成的封闭的凸多面体,C60就是其中的一种富勒烯,其结构如图所示,下列物质不属于富勒烯家族的是( )
目前,化学家们已经找到十余种富勒烯家族的Cn,它们分子结构中都由正五边形和正六边形构成的封闭的凸多面体,C60就是其中的一种富勒烯,其结构如图所示,下列物质不属于富勒烯家族的是( )| A. | C28 | B. | C44 | C. | C70 | D. | C105 |
18.下列关于苯的性质的说法中,正确的是( )
| A. | 苯不溶于水,密度比水大 | |
| B. | 苯在空气中燃烧产生大量的黑烟 | |
| C. | 苯与溴水能发生加成反应生成溴苯 | |
| D. | 苯分子中存在碳碳双键,故能使酸性KMnO4溶液褪色 |
6.用NA代表阿伏加德罗常数的值,下列有关说法正确的是( )
| A. | 3mol NO2与足量H2O反应,转移的电子数为NA | |
| B. | 常温常压下,22.4L氦气含有NA个氦原子 | |
| C. | 锂在氧气中燃烧,1 mol O2作氧化剂时得到的电子数为2NA | |
| D. | 常温常压下,17克NH3中含有共价键的数目为3NA |
16. 拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图,下列对该化合物叙述正确的是( )
拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图,下列对该化合物叙述正确的是( )
 拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图,下列对该化合物叙述正确的是( )
拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图,下列对该化合物叙述正确的是( )| A. | 属于芳香烃 | B. | 属于卤代烃 | C. | 属于芳香化合物 | D. | 属于酚类 |
3.下列关于物质性质的叙述中正确的是( )
| A. | Cl2能与金属活动性顺序表中大多数金属反应 | |
| B. | N2是大气中的主要成分之一,雷雨时可直接转化为NO2 | |
| C. | 硫是一种黄色的能溶于水的晶体,既有氧化性又有还原性 | |
| D. | 浓硫酸可以干燥Cl2,但不能干燥SO2 |
20.下列物质属于分子晶体的是( )
| A. | 熔点是1070℃,易溶于水,水溶液能导电 | |
| B. | 熔点是10.31℃,液态不导电,水溶液能导电 | |
| C. | 能溶于水,熔点812.8℃,沸点是1446℃ | |
| D. | 熔点是97.80℃,质软、导电,密度是0.97g/cm3 |