题目内容
氯气除了用实验室制取外,还可用KMnO4、KClO3氧化浓盐酸快速制取.根据上述反应原理,有人提出能否利用Na2O2的强氧化性氧化浓盐酸得到氯气呢?某课外小组在实验室进行了探索性实验,设计了如图装置:
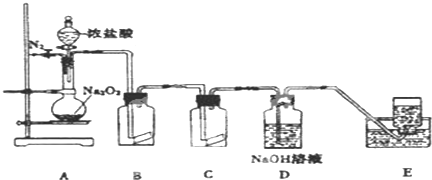
操作步骤及现象如下:
①组装好装置, ,加入药品.
②缓慢通入一定量的N2后,将装置E连接好(导管未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,反应剧烈,产生黄绿色气体.
③一段时间后,将导管末端伸入集气瓶中收集气体.装置E中收集到能使带火星的木条复燃的无色气体.
④反应结束后,关闭分液漏斗的活塞,再通入一定量的N2,至装置中气体无色.
回答下列问题:
(1)写出Na2O2的电子式
(2)写出实验室制取Cl2的离子方程式
(3)操作步骤①中组装好装置后的操作是 ,加入药品.
(4)装置B中湿润的红色布条褪色,说明A中有 (填化学式)生成,装置C中为湿润的KI-淀粉试纸,能否仅通过试纸变蓝证明上述结论,请用离子方程式说明原因 ;
(5)装置D的作用是 ;
(6)实验证明,Na2O2甚至能与干燥的HCl反应生成氯气,请完成该反应的化学方程式;
Na2O2+ HCl= Cl2+ NaCl+ .

操作步骤及现象如下:
①组装好装置,
②缓慢通入一定量的N2后,将装置E连接好(导管未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,反应剧烈,产生黄绿色气体.
③一段时间后,将导管末端伸入集气瓶中收集气体.装置E中收集到能使带火星的木条复燃的无色气体.
④反应结束后,关闭分液漏斗的活塞,再通入一定量的N2,至装置中气体无色.
回答下列问题:
(1)写出Na2O2的电子式
(2)写出实验室制取Cl2的离子方程式
(3)操作步骤①中组装好装置后的操作是
(4)装置B中湿润的红色布条褪色,说明A中有
(5)装置D的作用是
(6)实验证明,Na2O2甚至能与干燥的HCl反应生成氯气,请完成该反应的化学方程式;
考点:性质实验方案的设计
专题:实验设计题
分析:A装置制取氯气,B装置检验次氯酸的漂白性,C装置检验氯气的氧化性,D装置吸收氯气及氯化氢,E装置收集氧气.
(1)过氧化钠由钠离子和过氧根离子通过离子键结合形成;
(2)实验室通常用二氧化锰和浓盐酸共热制取氯气;
(3)组装仪器后需检查气密性再装药品;
(4)HClO有漂白性,氯气和水反应生成HClO;O2、Cl2都具有强氧化性,都能将碘离子氧化为I2,I2遇淀粉试液变蓝色;
(5)氢氧化钠可吸收酸性气体;
(6)根据元素守恒知,生成物中还有水生成,该反应中O元素化合价由-1价变为-2价、Cl元素化合价由-1价变为0价,根据转移电子相等配平方程式.
(1)过氧化钠由钠离子和过氧根离子通过离子键结合形成;
(2)实验室通常用二氧化锰和浓盐酸共热制取氯气;
(3)组装仪器后需检查气密性再装药品;
(4)HClO有漂白性,氯气和水反应生成HClO;O2、Cl2都具有强氧化性,都能将碘离子氧化为I2,I2遇淀粉试液变蓝色;
(5)氢氧化钠可吸收酸性气体;
(6)根据元素守恒知,生成物中还有水生成,该反应中O元素化合价由-1价变为-2价、Cl元素化合价由-1价变为0价,根据转移电子相等配平方程式.
解答:
解:(1)过氧化钠由钠离子和过氧根离子通过离子键结合形成,过氧根中氧和氧靠共价键结合,电子式为: ,故答案为:
,故答案为: ;
;
(2)实验室通常用二氧化锰和浓盐酸共热制取氯气,反应的离子方程式为:MnO2+2Cl-+4H+
Mn2++Cl2↑+2H2O,
故答案为:MnO2+2Cl-+4H+
Mn2++Cl2↑+2H2O;
(3)组装仪器后需检查气密性再装药品;故答案为:检查装置的气密性;
(4)装置B中湿润的红色布条褪色,说明有次氯酸生成,氯气和水反应生成次氯酸和盐酸,故A中生成了氯气;碘离子易被氧化,氧气可把碘离子氧化,反应方程式为:4H++O2+4I-=2I2+2H2O,故湿润的碘化钾-淀粉试纸变蓝不能说明有氯气生成,故答案为:Cl2;4H++O2+4I-=2I2+2H2O;
(5)进入装置D中的气体有挥发的氯化氢,没反应的氯气及氧气,氢氧化钠可吸收氯化氢和氯气,保证E中收集气体是无氯气、氯化氢的气体;故答案为:吸收HCl和过量的氯气防止污染空气使E中收集到较纯的氧气;
(6)根据元素守恒知,生成物中还有水生成,该反应中O元素化合价由-1价变为-2价、Cl元素化合价由-1价变为0价,根据转移电子相等配平方程式为Na2O2+4HCl═Cl2+2NaCl+2H2O,
故答案为:1;4;1;2;2H2O.
 ,故答案为:
,故答案为: ;
;(2)实验室通常用二氧化锰和浓盐酸共热制取氯气,反应的离子方程式为:MnO2+2Cl-+4H+
| ||
故答案为:MnO2+2Cl-+4H+
| ||
(3)组装仪器后需检查气密性再装药品;故答案为:检查装置的气密性;
(4)装置B中湿润的红色布条褪色,说明有次氯酸生成,氯气和水反应生成次氯酸和盐酸,故A中生成了氯气;碘离子易被氧化,氧气可把碘离子氧化,反应方程式为:4H++O2+4I-=2I2+2H2O,故湿润的碘化钾-淀粉试纸变蓝不能说明有氯气生成,故答案为:Cl2;4H++O2+4I-=2I2+2H2O;
(5)进入装置D中的气体有挥发的氯化氢,没反应的氯气及氧气,氢氧化钠可吸收氯化氢和氯气,保证E中收集气体是无氯气、氯化氢的气体;故答案为:吸收HCl和过量的氯气防止污染空气使E中收集到较纯的氧气;
(6)根据元素守恒知,生成物中还有水生成,该反应中O元素化合价由-1价变为-2价、Cl元素化合价由-1价变为0价,根据转移电子相等配平方程式为Na2O2+4HCl═Cl2+2NaCl+2H2O,
故答案为:1;4;1;2;2H2O.
点评:本题考查性质实验探究,侧重考查学生动手操作、分析问题能力,物质的性质是实验设计的依据,性质、制备实验方案设计是高考高频点,综合性较强,涉及知识点较多,熟练掌握元素化合物知识,题目难度中等.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
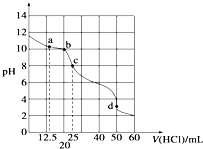 在常温下,0.100 0mol?L-1 Na2CO3溶液25mL用0.100 0mol?L-1盐酸滴定,其滴定曲线如图所示,对滴定过程中所得溶液中相关离子浓度间的关系,下列有关说法正确的是( )
在常温下,0.100 0mol?L-1 Na2CO3溶液25mL用0.100 0mol?L-1盐酸滴定,其滴定曲线如图所示,对滴定过程中所得溶液中相关离子浓度间的关系,下列有关说法正确的是( )| A、a点:c(CO32-)=c(HCO3-)>c(OH-) |
| B、b点:5c(Cl-)>4c(HCO3-)+4c(CO32-) |
| C、c点:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| D、d点:c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
对于反应KClO3+HCl=KC1+Cl2↑+H2O(未配平)若有0.1mol KClO3 参加反应,下列说法正确的是( )
| A、转移0.5 mol电子 |
| B、生成0.1 mol Cl2 |
| C、被氧化的HC1为0.6 mol |
| D、Cl2是只是氧化产物不是还原产物 |
下列各组溶液等体积混合后,所得溶液pH最大的是( )
| A、0.1mol?L-1NaHCO3溶液与0.1mol?L-1 NaOH溶液 |
| B、0.1mol?L-1NaHSO4溶液与0.1mol?L-1 Ba(OH)2溶液 |
| C、0.2mol?L-1氨水与0.1mol?L-1盐酸 |
| D、0.1mol?L-1氨水与0.1mol?L-1盐酸 |