题目内容
14.下列有关说法正确的是( )| A. | 0.5molH2SO4与0.5molBa(OH)2完全反应所放出的热量,即为中和热 | |
| B. | 加入催化剂,活化分子的百分含量和数目都增大,从而反应速率增大 | |
| C. | NaCl溶液能导电,所以NaCl溶液是电解质 | |
| D. | 牺牲阳极的阴极保护法,是根据电解原理防护金属腐蚀 |
分析 A.在稀溶液中,酸跟碱发生中和反应生成1 mol水且生成可溶性的盐时的反应热叫做中和热;
B.催化剂能降低反应所需活化能,使部分非活化分子转化为活化分子;
C.在水溶液里或熔融状态下能导电的化合物是电解质;
D.牺牲阳极的阴极保护法,是根据原电池原理防护金属腐蚀.
解答 解:A.在稀溶液中,酸跟碱发生中和反应生成1 mol水且生成可溶性的盐时的反应热叫做中和热,该反应中不仅生成1mol水还生成难溶性盐硫酸钡,且硫酸未标明是浓硫酸还是稀硫酸,故A错误;B.催化剂能降低反应所需活化能,使部分非活化分子转化为活化分子,从而活化分子的百分含量和数目都增大,导致反应速率增大,故B正确;
C.在水溶液里或熔融状态下能导电的化合物是电解质,氯化钠溶液是混合物,既不是电解质也不是非电解质,故C错误;
D.牺牲阳极的阴极保护法,是根据原电池原理防护金属腐蚀,外加电流的阴极保护法是根据电解原理保护金属腐蚀,故D错误;
故选B.
点评 本题考查中和热概念、化学反应速率影响因素、电解质概念、金属腐蚀与防护等知识点,为高频考点,侧重考查基本概念及基本原理,易错选项是B,注意:无论电解质还是非电解质都必须是化合物,为易错点.题目难度不大.

练习册系列答案
相关题目
5.下列有关铁及其化合物的说法中正确的是( )
| A. | 赤铁矿的主要成分是Fe3O4 | |
| B. | 铁与水蒸气在高温下的反应产物为Fe2O3和H2 | |
| C. | 除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤 | |
| D. | Fe3+与KSCN产生红色沉淀,铁与水蒸气在高温下的反应产物为Fe3O4和H2 |
9.下列实验室保存化学试剂的方法中,因试剂与容器反应而选用不当的是( )
| A. |  硫磺颗粒 | B. |  浓硝酸 | C. |  硫酸钠溶液 | D. |  硝酸银溶液 |
19.下列实验操作不会引起误差的是( )
| A. | 酸碱中和滴定时,用待测液润洗锥形瓶. | |
| B. | 酸碱中和滴定时,用冲洗干净的滴定管盛装标准溶液 | |
| C. | 用NaOH标准溶液测定未知度的盐酸时,选用酚酞作指示剂,实验时不小心多加了几滴 | |
| D. | 用标准盐酸测定未知浓度NaOH结束实验,酸式滴定管尖嘴部分有气泡,开始实验时无气泡 |
3.下列对化学用语的理解正确的是( )
| A. | 原子结构示意图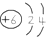 ,可以表示12C原子或13C原子 ,可以表示12C原子或13C原子 | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | 电子式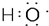 可以表示羟基或氢氧根离子 可以表示羟基或氢氧根离子 | |
| D. | CO2的比例模型: |
20.消除氮氧化物污染有多种方法.
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4 (g)+4NO2 (g)═4NO(g)+CO2(g)+2H2 O(g)△H=-574kJ•mol-1
②CH4 (g)+4NO(g)═2N2 (g)+CO2(g)+2H2 O(g)△H=-1160kJ•mol-1
③H2O(g)═H2O(l)△H=-44.0kJ•mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(1),△H=-955 kJ•mol-1.
(2)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2 (g)+CO2 (g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
①不能作为判断反应达到化学平衡状态的依据是B C
A.容器内CO2的浓度保持不变 B.v正(N2)=2v正(NO) C.容器内压强保持不变 D.混合气体的密度保持不变 E.混合气体的平均相对分子质量保持不变
②计算该温度下该反应的平衡常数为0.56(保留两位小数);
③在30min,改变某一条件,反应重新达到平衡,则改变的条件是减小CO2浓度.
(3)甲烷燃料电池可以提升能量利用率,如图是利用甲烷燃料电池电解50mL2mol/L的氯化铜溶液的装置示意图:
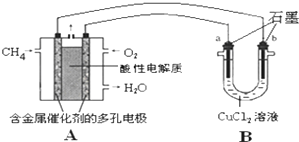
请回答:
①甲烷燃料电池的负极反应式是CH4-8e─+2H2O=CO2+8H+
②当A中消耗0.15mol氧气时,B中b(用a或b 表示)极增重19.2g.
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染.已知:
①CH4 (g)+4NO2 (g)═4NO(g)+CO2(g)+2H2 O(g)△H=-574kJ•mol-1
②CH4 (g)+4NO(g)═2N2 (g)+CO2(g)+2H2 O(g)△H=-1160kJ•mol-1
③H2O(g)═H2O(l)△H=-44.0kJ•mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(1),△H=-955 kJ•mol-1.
(2)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2 (g)+CO2 (g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
| 浓度/mol•L-1 时间/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
A.容器内CO2的浓度保持不变 B.v正(N2)=2v正(NO) C.容器内压强保持不变 D.混合气体的密度保持不变 E.混合气体的平均相对分子质量保持不变
②计算该温度下该反应的平衡常数为0.56(保留两位小数);
③在30min,改变某一条件,反应重新达到平衡,则改变的条件是减小CO2浓度.
(3)甲烷燃料电池可以提升能量利用率,如图是利用甲烷燃料电池电解50mL2mol/L的氯化铜溶液的装置示意图:

请回答:
①甲烷燃料电池的负极反应式是CH4-8e─+2H2O=CO2+8H+
②当A中消耗0.15mol氧气时,B中b(用a或b 表示)极增重19.2g.

 二氧化氯(ClO2)在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用如图所示装置模拟工业制取并收集ClO2.
二氧化氯(ClO2)在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用如图所示装置模拟工业制取并收集ClO2.