题目内容
18. 某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的0.1mol•L-1的盐酸中,试预测实验结果:K与盐酸反应最快.
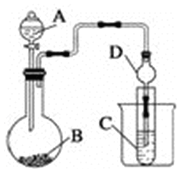
Ⅱ.利用下图装置可以验证非金属性的变化规律.
(2)仪器A的名称为分液漏斗,干燥管D的作用是防止倒吸.
(3)若要证明非金属性:S>C>Si,则A中加稀硫酸、B中加NaHCO3溶液、C中加Na2SiO3溶液,观察到C中溶液的现象为溶液变浑浊.
分析 I、(1)元素的金属性越强,其单质与酸或水反应越剧烈;
Ⅱ.(2)根据仪器的构造写出仪器A的名称;球形干燥管具有防止倒吸的作用;
(3)要证明非金属性:C>Si,可以通过二氧化碳和硅酸钠反应生成难溶性的硅酸来证明.
解答 解:I、(1)同一周期元素,金属性随着原子序数增大而减弱,元素的金属性越强,同一主族,原子序数越大,金属性越强,其单质与酸或水反应越剧烈,所以金属性K>Na>Mg>Al,则K与盐酸反应最剧烈,故答案为:K;
Ⅱ.(2)仪器A为分液漏斗,球形干燥管D能够防止倒吸,可以避免C中液体进入锥形瓶中,故答案为:分液漏斗;防止倒吸;
(3)若要证明非金属性:C>Si,可以通过二氧化碳和硅酸钠反应生成难溶性的硅酸来证明,由于B中加NaHCO3,故A中可以加硫酸,通过硫酸和碳酸氢钠的反应来制取CO2,然后的CO2通入C中的Na2SiO3中,可以发生反应:Na2SiO3+2CO2+2H2O=H2SiO3↓+2NaHCO3,离子反应为:SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3-,产生白色胶状沉淀,从而可以证明酸性:H2CO3>H2SiO3,故非金属性:C>Si.
故答案为:稀硫酸;Na2SiO3溶液;溶液变浑浊.
点评 本题考查了实验方案设计,涉及金属、非金属性强弱的探究,明确物质的性质是解本题关键,同时考查学生灵活运用知识解答问题的能力,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
8.“生物质”是指由植物或动物生命体衍生得到的物质的总称.作为人类解决能源危机重要途径之一的“生物质能”,主要指用树木、庄稼、草类等植物直接或间接提供的能量.下列说法不正确的是( )
| A. | 生物质能源是可再生的能源 | |
| B. | 生物质能来源于太阳能 | |
| C. | 使用沼气作为能源是利用生物质能的一种方式 | |
| D. | 生物质能的缺点是严重污染环境 |
9.下列化合物均为天然萜类化合物:
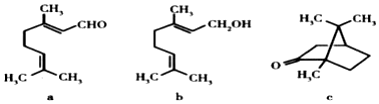
对这些萜类化合物叙述错误的是( )

对这些萜类化合物叙述错误的是( )
| A. | 三种化合物中只有a 和c 互为同分异构体 | |
| B. | 一定条件下a 和b可相互转化 | |
| C. | 三种化合物均易被氧化 | |
| D. | 三种化合物均可催化氢化 |
13.短周期元素的性质递变规律如图所示,下列说法正确的是( )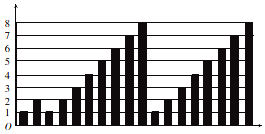

| A. | 横坐标为质子数,纵坐标为元素的最高正价 | |
| B. | 横坐标为原子序数,纵坐标为元素原子的最外层电子数 | |
| C. | 横坐标为核电荷数,纵坐标为元素原子的半径 | |
| D. | 横坐标为中子数,纵坐标为元素的非金属性 |
3.下列实验中不能观察到明显变化的是( )
| A. | 把溴水滴加到淀粉KI溶液中 | |
| B. | 把Cl2通入FeCl2溶液中 | |
| C. | 把绿豆大的钾投入少量水中 | |
| D. | 把一段打磨过的镁带放入少量冷水中 |
10.下列实验装置或者操作正确的是 ( )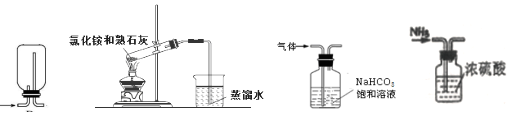

| A. | 排空气法收集氨气 | B. | 制氨水 | ||
| C. | 除二氧化碳中的少量二氧化硫 | D. | 干燥NH3 |
12.下列物质中不能由两种单质直接化合得到的是( )
| A. | FeCl3 | B. | Cu2S | C. | SO3 | D. | NH3 |

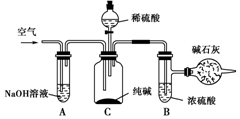 工业纯碱中常含有NaCl、Na2SO4等杂质,可用如图所示的装置测定工业纯碱中有效成分的含量.
工业纯碱中常含有NaCl、Na2SO4等杂质,可用如图所示的装置测定工业纯碱中有效成分的含量.