题目内容
设NA为阿伏伽德罗常数,下列说法正确的是( )
| A、标准状况下NA个SO3的体积为22.4 L |
| B、1mol Fe与足量的HCl反应,转移的电子数为3NA |
| C、2L 1mol/L的 H3PO4溶液中所含的H+数为6NA |
| D、标准状况下22.4L Cl2通入足量的石灰乳制备漂白粉,转移电子数为1 NA |
考点:阿伏加德罗常数
专题:
分析:A.气体摩尔体积只适用于气体;
B.铁与盐酸反应生成氯化亚铁;
C.磷酸为弱电解质,部分电离;
D.1mol Cl2通入足量的石灰乳中转移1mol的电子,标准状况下,11.2L Cl2的物质的量为0.5mol,所以转移电子数为0.5NA.
B.铁与盐酸反应生成氯化亚铁;
C.磷酸为弱电解质,部分电离;
D.1mol Cl2通入足量的石灰乳中转移1mol的电子,标准状况下,11.2L Cl2的物质的量为0.5mol,所以转移电子数为0.5NA.
解答:
解:A.标况下三氧化硫为液态,不能使用气体摩尔体积,故A错误;
B.铁与盐酸反应生成氯化亚铁,1mol Fe与足量的HCl反应,转移的电子数为2NA,故B错误;
C.磷酸为弱电解质,部分电离,2L 1mol/L的 H3PO4溶液中所含的H+数小于6NA,故C错误;
D.1mol Cl2通入足量的石灰乳中转移1mol的电子,标准状况下,11.2L Cl2的物质的量为0.5mol,所以转移电子数为0.5NA,故D正确;
故选:D.
B.铁与盐酸反应生成氯化亚铁,1mol Fe与足量的HCl反应,转移的电子数为2NA,故B错误;
C.磷酸为弱电解质,部分电离,2L 1mol/L的 H3PO4溶液中所含的H+数小于6NA,故C错误;
D.1mol Cl2通入足量的石灰乳中转移1mol的电子,标准状况下,11.2L Cl2的物质的量为0.5mol,所以转移电子数为0.5NA,故D正确;
故选:D.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,注意气体摩尔体积的使用条件与范围.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列除去杂质的方法正确的是( )
| A、除去N2中的少量O2:通过灼热的CuO粉末,收集气体 |
| B、除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
| C、除去CO2中的少量HCl:通入Na2CO3溶液,收集气体 |
| D、除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤 |
下列物质中,在一定条件下既能发生水解反应,又能发生银镜反应的是( )
| A、葡萄糖 | B、蛋白质 |
| C、甲酸甲酯 | D、苯甲醛 |
用NA表示阿伏德罗常数,下列叙述一定正确的是( )
| A、标准状况下,2.24LH2O含有的质子数为NA |
| B、等物质的量的氮气和氧气,都含有2NA个原子 |
| C、常温常压下,1.06gNa2CO3含有的Na+离子数为0.02 NA |
| D、物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为 NA |
下列说法正确的是( )
| A、某溶液加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有HCO3-或CO32- |
| B、明矾[KAl(SO4)2?12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
| C、欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 |
| D、将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色 |
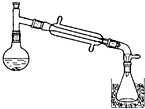 一溴乙烷为无色液体,熔点-119.1℃,沸点38.4℃,常用于汽油的乙基化、冷冻剂和麻醉剂.制备一溴乙烷的反应原理为:NaBr+H2SO4═HBr↑+NaHSO4,CH3CH2OH+HBr→CH3CH2Br+H2O.实验室可用如图装置制备一溴乙烷
一溴乙烷为无色液体,熔点-119.1℃,沸点38.4℃,常用于汽油的乙基化、冷冻剂和麻醉剂.制备一溴乙烷的反应原理为:NaBr+H2SO4═HBr↑+NaHSO4,CH3CH2OH+HBr→CH3CH2Br+H2O.实验室可用如图装置制备一溴乙烷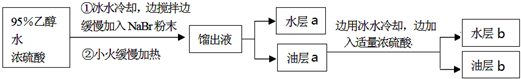
 在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:2MnO
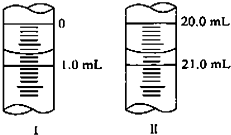
在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:2MnO (如图)(1)图Ⅰ表示10mL量筒中液面的位置,A与B、B与C刻度相差1mL,如果刻度A为5,量筒中液体体积是
(如图)(1)图Ⅰ表示10mL量筒中液面的位置,A与B、B与C刻度相差1mL,如果刻度A为5,量筒中液体体积是