题目内容
17.NA为阿伏加德罗常数,下列说法正确的是( )| A. | 标准状况下,11.2L的戊烷所含的分子数大于0.5NA | |
| B. | 28g乙烯所含共用电子对数目为4NA | |
| C. | 标准状况下,11.2 L二氯甲烷所含分子数为0.5NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为2NA |
分析 A.标况下,戊烷为液体,密度约为0.6g/ml;
B.求出乙烯的物质的量,然后根据1mol乙烯含6mol共用电子对来分析;
C.气体摩尔体积使用对象为气体;
D.乙烯、丙烯、丁烯的最简式为CH2,根据最简式计算出混合物中含有的原子数目.
解答 解:A.标准状况下,11.2L的戊烷质量约为11.2×1000mL×0.6g/ml=18666.6g,物质的量约为$\frac{18666.7g}{72g/mol}$>0.5NA,故A正确;
B.28g乙烯的物质的量为1mol,而1mol乙烯含6mol共用电子对,故B错误;
C.标况下,二氯甲烷为液体,不能使用气体摩尔体积,故C错误;
D.14g乙烯、丙烯、丁烯的混合气体中含有1mol最简式CH2,含有1molC、2molH,总共含有3mol原子,含有的原子数为3NA,故D错误;
故选:A.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,注意气体摩尔体积使用条件和对象.

练习册系列答案
相关题目
8.某有机物是甲酸和乙醇反应后生成物的同分异构体,此有机物是( )
| A. | 甲酸乙酯 | B. | 乙酸甲酯 | C. | 乙二酸 | D. | 丁酸 |
5.卤代烃能够发生下列反应:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr.下列有机物可合成环丙烷的是( )
| A. | CH3CH2CH2Cl | B. | CH3CHBrCH2Br | C. | CH2BrCH2CH2Br | D. | CH3CHBrCH2CH2Br |
12.下列说法正确的是( )
①标准状况下,6.02×1023个分子所占的体积约是22.4L
②0.5mol H2所占体积为11.2L
③标准状况下,1mol CCl4的体积为22.4L
④标准状况下,28g CO与N2的混合气体的体积约为22.4L
⑤各种气体的气体摩尔体积都约为22.4L•mol-1
⑥标准状况下,体积相同的气体的分子数相同.
①标准状况下,6.02×1023个分子所占的体积约是22.4L
②0.5mol H2所占体积为11.2L
③标准状况下,1mol CCl4的体积为22.4L
④标准状况下,28g CO与N2的混合气体的体积约为22.4L
⑤各种气体的气体摩尔体积都约为22.4L•mol-1
⑥标准状况下,体积相同的气体的分子数相同.
| A. | ①③⑤ | B. | ④⑥ | C. | ③④⑥ | D. | ①④⑥ |
2.在下列过程中,浓硫酸既表现强氧化性,又表现强酸性的是( )
| A. | 用浓硫酸做干燥剂 | |
| B. | 将火柴梗插入浓硫酸中,火柴梗很快变黑 | |
| C. | 铜与浓硫酸加热时发生反应 | |
| D. | 锌与稀硫酸发生置换反应制取氢气 |
9.实验室用二氧化锰和浓盐酸制取氯气时,最佳的除杂试剂和方法是( )
| A. | 水、浓H2SO4、洗气 | B. | 饱和NaHCO3溶液、浓H2SO4、洗气 | ||
| C. | 饱和NaCl溶液、浓H2SO4、洗气 | D. | NaOH溶液、浓H2SO4、洗气 |
6.下列符合化学实验“绿色化”的有( )
①在萃取操作的演示实验中,将CCl4萃取溴水改为CCl4萃取碘水
②汞不慎洒落地面时,要先用硫磺粉覆盖,使其化合成硫化汞后再妥善处理
③将实验室的废酸与废碱中和后再排放.
①在萃取操作的演示实验中,将CCl4萃取溴水改为CCl4萃取碘水
②汞不慎洒落地面时,要先用硫磺粉覆盖,使其化合成硫化汞后再妥善处理
③将实验室的废酸与废碱中和后再排放.
| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |
7.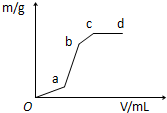 向用盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入的体积V之间的关系,关于图曲线的推测正确的是( )
向用盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入的体积V之间的关系,关于图曲线的推测正确的是( )
 向用盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入的体积V之间的关系,关于图曲线的推测正确的是( )
向用盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入的体积V之间的关系,关于图曲线的推测正确的是( )| A. | ab段产生的沉淀为硫酸钡 | |
| B. | ab产生段的沉淀为氢氧化镁 | |
| C. | bc段产生的沉淀为氢氧化镁 | |
| D. | bc段产生的沉淀为硫酸钡和氢氧化镁 |
