题目内容
5.1.8克水中所含的水分子数是( )| A. | 0.1摩尔 | B. | 6.02×1023个 | C. | 18个 | D. | 1摩尔 |
分析 根据水的摩尔质量可以求出1.8g水的物质的量,然后再计算含有的分子的个数.
解答 解:水的摩尔质量为18g/mol,水分子的个数:N=m/M×NA=$\frac{1.8}{18}$×6.02×1023=6.02×1022个=0.1mol.
故选A.
点评 该题考查应用阿伏伽德罗常数进行有关的计算,关键是要知道物质的量的计算方法,属于基础知识、简单题目.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列有关化学用语表示正确的是( )
| A. | -CHO的电子式: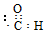 | B. | 聚丙烯的结构简式: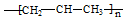 | ||
| C. | 1-丁烯的键线式: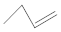 | D. | 丙烷分子的比例模型为: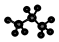 |
16.下列表述正确的是( )
| A. | 某离子第三层上和第二层上的电子数均为第一层的 4 倍 | |
| B. | Cl-的结构示意图: | |
| C. | 某物质的焰色反应为黄色,某物质一定为钠的化合物 | |
| D. | 14C 和 14N 的质量数相等,互称为同位素 |
13.20mL浓硝酸和2.56g铜反应,铜完全溶解,生成的气体颜色由深变浅(生成NO2、NO),共收集到1.12L气体(标准状况),剩余酸用NaOH中和,共耗去1mol/L氢氧化钠30mL.则浓HNO3物质的量浓度为( )
| A. | 8 mol/L | B. | 9 mol/L | C. | 11 mol/L | D. | 12 mol/L |
10.下列化学用语表示正确的是( )
| A. | 1H、2H、3H互为同素异形体 | |
| B. | CO2的比例模型: | |
| C. | NaHCO3在水溶液中的电离方程式:NaHCO3?Na++HCO3-HCO3-?H++CO32- | |
| D. | 次氯酸的电子式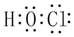 |
17.在某温度下,可逆反应mA(g)+nB(g)?pC(g)+qD(g)平衡常数为K,下列说法正确的是( )
| A. | K越大,达到平衡时,反应进行的越完全 | |
| B. | K随反应物浓度的改变而改变 | |
| C. | K越小,达到平衡时,反应物的转化率越大 | |
| D. | K不随温度的升高而改变 |
14.在稀硫酸中加入铜粉,铜粉不溶解,再加入下列固体粉末:
①FeCl2
②Fe2O3
③Zn
④Fe2(SO)3
⑤AgNO3
可使铜粉溶解的是( )
①FeCl2
②Fe2O3
③Zn
④Fe2(SO)3
⑤AgNO3
可使铜粉溶解的是( )
| A. | ①②③ | B. | ②③④ | C. | ③④⑤ | D. | ②④⑤ |
15.某下组同学欲研究SO2的性质.
(1)将相关的含硫物质分为如下表所示3组.第3组中物质X的化学式是H2SO4.
(2)利用如图所示的装置研究SO2的性质:
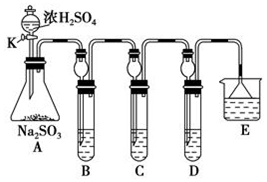
①在B中检验SO2的氧化性,则B中发生的化学反应方程式:SO2+2H2S=3S↓+2H2O.
②在C中装KMnO4溶液,目的是检验SO2的还原性,溶液逐渐褪色.生成Mn2+.同时pH降低.则C中反应的离子方程式为5SO2+2H2O+2MnO4-=5SO42-+2Mn2++4H+.
③在D中有40mL2.5mol/LNaOH溶液,反应后增重4,则装置D中发生反应的总化学方程式是5SO2+8NaOH=3Na2SO3+2NaHSO3+3H2O.
(1)将相关的含硫物质分为如下表所示3组.第3组中物质X的化学式是H2SO4.
| 第1组 | 第2组 | 第3组 |
| S(单质) | SO2、H2SO4、Na2SO3、NaHSO3 | SO3、X、Na2SO4、NaHSO4 |

①在B中检验SO2的氧化性,则B中发生的化学反应方程式:SO2+2H2S=3S↓+2H2O.
②在C中装KMnO4溶液,目的是检验SO2的还原性,溶液逐渐褪色.生成Mn2+.同时pH降低.则C中反应的离子方程式为5SO2+2H2O+2MnO4-=5SO42-+2Mn2++4H+.
③在D中有40mL2.5mol/LNaOH溶液,反应后增重4,则装置D中发生反应的总化学方程式是5SO2+8NaOH=3Na2SO3+2NaHSO3+3H2O.