题目内容
某有机物A有C、H、O三种元素组成,现取18g A在足量O2中充分燃烧,将燃烧产物全部依次通过无水氯化钙和碱石灰后,固体质量的增加依次为10.8g和26.4g,求:
(1)A的最简式是
(2)若常温下A是气体,则A的结构式是
 .
.
(3)若0.1mol A含4.8g氧,A在浓硫酸作用下能生成六元环状化合物,写出该反应的化学方程式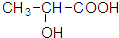
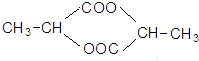 +2H2O
+2H2O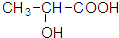
 +2H2O.
+2H2O.
(1)A的最简式是
CH2O
CH2O
.(2)若常温下A是气体,则A的结构式是


(3)若0.1mol A含4.8g氧,A在浓硫酸作用下能生成六元环状化合物,写出该反应的化学方程式
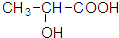
| 浓硫酸 |
| △ |
 +2H2O
+2H2O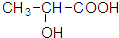
| 浓硫酸 |
| △ |
 +2H2O
+2H2O分析:无水氯化钙增重的质量为水的质量,n(H2O)=
=0.6mol,碱石灰增重的质量为CO2的质量,n(CO2)=
=0.6mol,则有机物中m(C)=0.6mol×12g/mol=7.2g,m(H)=1.2g,m(O)=18g-7.2g-1.2g=9.6g,所以18g有机物中含有n(O)=
=0.6mol,则有机物中N(C):N(H):N(O)=0.6:1.2:0.6=1:2:1,最简式为CH2O,最简式为CH2O的有甲醛、乙酸、乳酸、葡萄糖等,结合对应有机物的性质解答该题,
| 10.8g |
| 18g/mol |
| 26.4g |
| 44g/mol |
| 9.6g |
| 16g/mol |
解答:解:无水氯化钙增重的质量为水的质量,n(H2O)=
=0.6mol,碱石灰增重的质量为CO2的质量,n(CO2)=
=0.6mol,则有机物中m(C)=0.6mol×12g/mol=7.2g,m(H)=1.2g,m(O)=18g-7.2g-1.2g=9.6g,所以18g有机物中含有n(O)=
=0.6mol,则有机物中N(C):N(H):N(O)=0.6:1.2:0.6=1:2:1,最简式为CH2O,最简式为CH2O的有甲醛、乙酸、乳酸、葡萄糖等,
(1)由以上分析可知该有机物的最简式为CH2O,故答案为:CH2O;
(2)若常温下A是气体,应为甲醛,结构式是 ,故答案为:
,故答案为: ;
;
(3)0.1molA含4.8g氧,即n(O)=
=0.3mol,说明分子中含有3个O原子,A在浓硫酸作用下能生成六元环状化合物,则含有1个-COOH、-OH,A为乳酸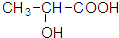 ,该反应方程式为:
,该反应方程式为: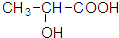
 +2H2O,
+2H2O,
故答案为: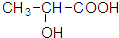
 +2H2O.
+2H2O.
| 10.8g |
| 18g/mol |
| 26.4g |
| 44g/mol |
| 9.6g |
| 16g/mol |
(1)由以上分析可知该有机物的最简式为CH2O,故答案为:CH2O;
(2)若常温下A是气体,应为甲醛,结构式是
 ,故答案为:
,故答案为: ;
;(3)0.1molA含4.8g氧,即n(O)=
| 4.8g |
| 16g/mol |
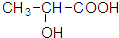 ,该反应方程式为:
,该反应方程式为: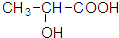
| 浓硫酸 |
| △ |
 +2H2O,
+2H2O,故答案为:
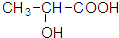
| 浓硫酸 |
| △ |
 +2H2O.
+2H2O.点评:本题考查有机物的推断,侧重于有机物燃烧的规律的计算,注意最简式为CH2O的有机物的种类,结合对应有机物的性质解答该题,题目难度中等.

练习册系列答案
相关题目




