题目内容
下列反应的离子方程式不正确的是( )
| A、0.1mol FeBr2中滴入含Cl2 0.1mol氯水:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | ||||
| B、向氢氧化钙溶液中加入少量碳酸氢钠溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | ||||
| C、向Ca(HCO3)2溶液中滴加少量Ca(OH)2溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | ||||
D、向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全并加热溶液Ba2++2OH-+H++SO42-+NH4+
|
考点:离子方程式的书写
专题:离子反应专题
分析:A.由电子守恒可知,亚铁离子全部被氧化,而溴离子一半被氧化;
B.少量碳酸氢钠完全反应,生成碳酸钙、水、NaOH;
C.反应生成碳酸钙和水;
D.至刚好沉淀完全并加热,二者以1:1反应,反应生成硫酸钡、水、氨气.
B.少量碳酸氢钠完全反应,生成碳酸钙、水、NaOH;
C.反应生成碳酸钙和水;
D.至刚好沉淀完全并加热,二者以1:1反应,反应生成硫酸钡、水、氨气.
解答:
解:A.0.1mol FeBr2中滴入含Cl2 0.1mol氯水的离子反应为2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl-,故A错误;
B.向氢氧化钙溶液中加入少量碳酸氢钠溶液的离子反应为Ca2++HCO3-+OH-═CaCO3↓+H2O,故B正确;
C.向Ca(HCO3)2溶液中滴加少量Ca(OH)2溶液的离子反应为Ca2++HCO3-+OH-═CaCO3↓+H2O,故C正确;
D.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全并加热溶液的离子反应为Ba2++2OH-+H++SO42-+NH4+
BaSO4↓+NH3↑+2H2O,故D正确;
故选A.
B.向氢氧化钙溶液中加入少量碳酸氢钠溶液的离子反应为Ca2++HCO3-+OH-═CaCO3↓+H2O,故B正确;
C.向Ca(HCO3)2溶液中滴加少量Ca(OH)2溶液的离子反应为Ca2++HCO3-+OH-═CaCO3↓+H2O,故C正确;
D.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全并加热溶液的离子反应为Ba2++2OH-+H++SO42-+NH4+
| ||
故选A.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的化学反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及与量有关的离子反应的考查,题目难度不大.

练习册系列答案
相关题目
一种新型燃料电池,是用两根金属铂做电极插入KOH溶液中,然后向两极上分别通入CH3OH和O2,下解说法不正确的是( )
| A、通入CH3OH的电极为负极 |
| B、随着放电的进行,负极附近pH上升 |
| C、每消耗1mol CH3OH可以向外电路提供6mol e- |
| D、通入O2的一极电极反应为4H2O+2O2-+8e-═8OH- |
在一个固定容积的密闭容器中,可逆反应:mA(g)+nB(g)?pC(g)+qD(g)中,当m、n、p、q为任意正整数时,达到平衡的标志是( )
| A、体系压强不再发生变化 |
| B、反应速率vA:vB:vC:vD=m:n:p:q |
| C、容器内气体的密度不再改变 |
| D、各组分的物质的量浓度不再改变 |
下列叙述不正确的是( )
| A、与28 gCO具有相同分子数的C2H4的质量一定是28 g |
| B、1 molAl3+含有的核外电子数为3NA |
| C、常温常压下,1 molL甲烷含有的原子数为5NA |
| D、1 L 1 mol?L-1醋酸溶液中CH3COO+的数目小于NA |
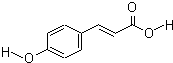 对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛.结构简式如图:
对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛.结构简式如图: 氨作为一种富氢化合物,具有各种优点,特别是氨有着良好的产业基础,价格低廉,氨作为燃料电池燃料具有很大的发展潜力.读氨氧燃料电池示意图,回答下列问题:
氨作为一种富氢化合物,具有各种优点,特别是氨有着良好的产业基础,价格低廉,氨作为燃料电池燃料具有很大的发展潜力.读氨氧燃料电池示意图,回答下列问题: